Приём гормона Тироксина — мифы

? Часто мы слышим выражение «Подсадили на гормоны. », в особенности в отношении Тироксина. Прием гормона тироксина (он же Эутирокс, он же Л-тироксин), связан со множеством мифов.
Самые частые?: «Вот сейчас подсадят, и не слезу с него до конца жизни» или «Я его так долго пью, он не вредит мне?»
Подробнее о мифах тироксина врач эндокринолог нашего медицинского центра в г. Нур-Султан Талышканова Т.Н.

Вот только гормоны это не «наркотики», на которые подсаживаются и не «химия», с которой не слезть.
Что же такое тироксин?
Это гормон, который вырабатывает наша щитовидная железа. При его недостатке (по причине заболеваний щитовидной железы) — развивается гипотиреоз.
А что такое эутирокс? Л-тироксин?
Это абсолютный аналог нашего гормона тироксина. Да, вещество получено синтетическим путем, а не выделено из щитовидки барана?/теленка? или еще кого-то, но формула вещества НИЧЕМ не отличается от нашего собственного тироксина.
? Препарат абсолютно безопасен при беременности?/кормлении??/детям с рождения ?и людям любого возраста и пола?.
⏰ Что касается пожизненного или временного приема тироксина — все решается строго индивидуально.
В ряде случаев действительно необходим пожизненный прием и терапию невозможно отменить. Но нередко, бывает и так, что отмена препарата возможна и пациент в нем больше не нуждается.
Все зависит от клинической картины, выраженности гипотиреоза и еще массы факторов.
Ну в заключении, мое любимое: «Доктор сказал мне пить тироксин в 5-6 утра/или/с 6 до 8 утра/или/я ставлю будильник на 7 утра,чтоб его выпить!!» ?
?Спешу вас обрадовать — это очередной миф и выдумки.
Тироксин всасывается натощак (то есть когда вы голодны и вашем желудке нет еды), поэтому пить его вы можете хоть в 6/7/8/9/10 утра (как вам удобно) за 30 минут до приема пищи.
Вот и все?
Всегда рады помочь вам в нашей клинике «Medi-art ❤
Глава VII. Физиология теплообмена
Понятие о гомойотермии и пойкилотермии
Жизнедеятельность животного и человека связана с постоянным потреблением энергии, которую организм получает за счет поступления и переработки питательных веществ. Химические превращения, протекающие в клетках организма в процессе обмена веществ, сопровождаются теплообразованием.
Животных с постоянной температурой тела называют гомойотермными (теплокровными). Относительное постоянство температуры тела у таких животных обеспечивается изменением теплопродукции и теплоотдачи.
Постоянство температуры тела называют изотермией. Значение изотермии заключается в том, что она обеспечивает независимость обменных процессов в тканях и органах от колебаний температуры окружающей среды. Человек является теплокровным существом.
Температура тела человека
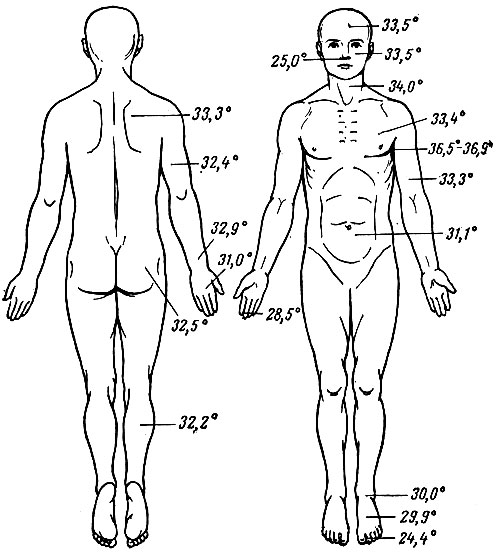
Рис. 38. Температура кожи разных участков тела человека
Температура внутренних органов более высокая, поэтому сложилось представление об «оболочке» и «ядре» тела, «Оболочка» тела имеет более низкую температуру, которая подвержена значительным колебаниям. В состав «оболочки» входят кожа, скелетные мышцы. Установлено, что температура мышечной ткани в состоянии покоя и работы может колебаться в пределах 7°С. «Ядро» тела имеет более высокую температуру, колебания которой сравнительно невелики. «Ядро» включает внутренние органы. Температура внутренних органов зависит от интенсивности обменных процессов. Наиболее интенсивно обменные процессы протекают в печени, которая является самым «горячим» органом тела: температура в ткани печени равна 38-38,5°С. Температура в прямой кишке составляет 37-37,5°С. Однако она может колебаться в пределах 4-5°С в зависимости от наличия в ней каловых масс, кровенаполнения ее слизистой оболочки и других причин. У бегунов на длинные (марафонские) дистанции в конце состязаний температура в прямой кишке может повышаться до 39-40°С.
Теплопродукция и теплоотдача, их компенсаторные изменения
Тепловой обмен в животном организме тесно связан с энергетическим. При окислении органических веществ, например глюкозы, пировиноградной кислоты, выделяется энергия. Часть этой энергии рассеивается в виде тепла и не может быть использована организмом для совершения какой-либо работы. Другая часть энергии идет на синтез АТФ. Молекулы АТФ, как уже указывалось, обладают способностью аккумулировать энергию. Эта потенциальная энергия может быть использована организмом в его деятельности.
Разобщение окислительного фосфорилирования может произойти, например, под влиянием гормонов щитовидной железы. В этом случае для образования достаточного количества АТФ окислительные процессы должны протекать более интенсивно, а значительная часть выделяющейся энергии рассеивается в виде тепла.
Таким образом, соотношение теплового и энергетического обмена определяется изменением направленности окислительных процессов в организме.
Источником тепла в организме являются все ткани. Кровь, протекая через ткани, нагревается. Некоторые органы, например печень, скелетные мышцы, отдают крови больше тепла, чем другие. Общее количество тепла, получаемое кровью, равно суммарному количеству тепла, выделяющегося всеми тканями.
Физическая терморегуляция. Этот процесс осуществляется за счет отдачи тепла во внешнюю среду путем конвекции (теплопроведения), радиации (теплоизлучения) и испарения воды.
Конвекция (теплопроведение) заключается в непосредственной отдаче тепла прилегающим к коже предметам или частицам среды. Отдача тепла тем интенсивнее, чем больше разница температур между поверхностью тела и окружающим воздухом. Чем холоднее воздух, тем сильнее он охлаждает кожу. Если же воздух теплее кожи, то проведение тепла будет идти в противоположном направлении, это вызовет повышение температуры кожи.
Интенсивность отдачи тепла во многом зависит от теплопроводности окружающей среды. В воде отдача тепла происходит быстрее, чем на воздухе. Одежда уменьшает или даже прекращает теплопроведение.
В состоянии относительного покоя взрослый человек выделяет во внешнюю среду 15% тепла путем теплопроведения, около 66% посредством теплоизлучения и 19% за счет испарения воды.
При повышении температуры окружающей среды, при физической нагрузке потоотделение увеличивается. Человек способен в сутки выделить до 10-15 л жидкости с потом. В среднем же человек теряет за сутки около 0,8 л пота, а с ним 2,1 мДж (500 ккал) тепли.
При дыхании человек также выделяет ежесуточно около 0,5 л воды. Энергия при этом тратится не только на испарение воды с поверхности дыхательных путей, но и на согревание выдыхаемого воздуха. При физической работе вентиляция легких увеличивается, а это приводит к повышению теплоотдачи.
При низкой температуре окружающей среды (15°С и ниже) около 90% суточной теплоотдачи происходит за счет теплопроведения и теплоизлучения. В этих условиях видимого потоотделения не происходит.
У человека большую роль в изменении теплоотдачи играет выбор одежды в зависимости от температуры окружающей среды. Мало проницаемая для паров воды одежда препятствует эффективному потоотделению и может служить причиной перегревания организма человека.
В горячих цехах, в жарких странах, при длительных походах человек теряет большое количество жидкости с потом. При этом появляется чувство жажды, которое не утоляется водой. Это связано с тем, что с потом теряется большое количество минеральных солей. Если добавить к питьевой воде соль, то чувство жажды исчезнет и самочувствие людей улучшится.
Таким образом, постоянство температуры тела человека обеспечивается механизмами физической и химической терморегуляции.
Центры регуляции теплообмена, их афферентные и эфферентные связи
Организм должен обеспечивать постоянство температуры не только в покое и при комфортной температуре (18-22°С), но и при различных нагрузках, а также при изменении температуры окружающей среды. Для этого организм человека располагает специальными физиологическими механизмами, регулирующими температуру тела.
Терморегуляция осуществляется рефлекторно. Колебания температуры окружающей среды воспринимаются особыми рецепторами, получившими название терморецепторов. В большом количестве терморецепторы располагаются в коже, слизистой оболочке полости рта, верхних дыхательных путях. Обнаружены терморецепторы во внутренних органах, венах, а также в некоторых образованиях центральной нервной системы.
Нервные импульсы, возникающие в терморецепторах, по афферентным нервным волокнам поступают в спинной мозг. По проводящим путям они достигают зрительных бугров, а от них идут в гипоталамическую область и к коре головного мозга. В коре головного мозга возникают ощущения тепла или холода.
Спинной мозг является проводником нервных импульсов не только от терморецепторов к головному мозгу, но и от головного мозга к мышцам, сосудам, потовым железам. В спинном мозге находятся центры некоторых терморегуляторных рефлексов. Однако одних спинальных терморегуляторных механизмов недостаточно для обеспечения постоянства температуры тела.
Гипоталамус является основным рефлекторным центром теплорегуляции. Нейроны гипоталамуса возбуждаются под влиянием нервных импульсов, поступающих от терморецепторов. В гипоталамусе обнаружены собственные терморецепторы, которые возбуждаются в ответ на изменение температуры крови (улавливают изменения температуры на сотые доли градуса).
При разрушении гипоталамической области гомойотермные животные теряют способность поддерживать постоянную температуру тела и становятся пойкилотермными. Установлено, что передние отделы гипоталамуса контролируют механизмы физической терморегуляции (за счет изменения тонуса кровеносных сосудов и интенсивности потоотделения), т. е. они являются центром теплоотдачи. При их разрушении животные хорошо переносят холод, но быстро перегреваются при повышении температуры окружающей среды. Задние отделы гипоталамуса контролируют химическую терморегуляцию и являются центром теплообразования. При их разрушении животные не переносят холод, так как не происходит компенсаторного повышения теплообразования.
Важная роль в регуляции температуры тела принадлежит коре головного мозга. В лаборатории К. М. Быкова в опытах на собаках установлена возможность условнорефлекторных изменений теплоотдачи и теплопродукции. Собаку неоднократно помещали в комнату с температурой воздуха 22°С. У животного увеличивалась теплоотдача (учащалось дыхание, собака высовывала язык, что увеличивало испарение слюны). Затем собаку приводили в эту же комнату, но температура воздуха в ней была равна 10°С. В данных условиях у животного также возникало увеличение отдачи тепла, несмотря на низкую температуру окружающей среды, т. е. у собаки возник условный терморегуляционный рефлекс на обстановку комнаты.
Эфферентными нервами центра теплорегуляции являются главным образом симпатические волокна. Если разрушить симпатическую нервную систему (произвести десимпатизацию), то раздражение центров теплорегуляции гипоталамуса не вызовет изменения температуры тела.
В регуляции теплообмена участвует и гормональный механизм, в частности гормоны щитовидной железы и надпочечников. Гормон щитовидной железы тироксин, повышая обмен веществ в организме, увеличивает теплообразование. Поступление тироксина в кровь возрастает при охлаждении организма. Гормон надпочечников адреналин усиливает окислительные процессы, увеличивая тем самым теплообразование. Кроме того, адреналин суживает сосуды, в частности кожи, и за счет этого уменьшается теплоотдача.
Рассмотрим механизмы, которые обеспечивают приспособление организма к пониженной температуре окружающей среды. При понижении температуры окружающей среды происходит рефлекторное возбуждение гипоталамуса. Повышение его активности стимулирует гипофиз, результатом чего является усиленное выделение тиреотропного и адренокортикотропного гормонов. Эти гормоны повышают активность соответственно щитовидной железы и надпочечников. Гормоны данных желез стимулируют теплопродукцию, а адреналин, кроме того, суживая сосуды, уменьшает теплоотдачу.
Таким образом, при охлаждении включаются защитные механизмы организма, повышающие обмен веществ, теплообразование и уменьшающие теплоотдачу.
Регуляция обмена веществ и энергии
Нервная система регулирует обменные, энергетические и тепловые процессы в организме. Впервые это было показано в опытах Клода Бернара и И. П. Павлова. В середине прошлого века Клод Бернар, произведя укол иглой в дно IV желудочка продолговатого мозга кролика, обнаружил резкое повышение уровня сахара в крови и появление его в моче. Этот опыт получил название «сахарный укол». Впоследствии было показано, что «сахарный укол» нарушает не только углеводный, но и другие виды обмена. Под влиянием этого вмешательства у животных понижается температура печени, мышц, кишечника, повышается интенсивность белкового обмена, что сопровождается увеличенным выделением азота с мочой.
В дальнейшем была установлена возможность условнорефлекторных изменений уровня обмена веществ. Если многократно сочетать прием человеком сахара с одновременным включением метронома, то через некоторое время изолированное применение условного сигнала приводит к повышению содержания сахара в крови. Условнорефлекторный механизм изменения обмена веществ и энергии наблюдается у человека в предстартовых и предрабочих состояниях. У спортсменов до начала соревнования, а у рабочего перед работой отмечается повышение обмена веществ, температуры тела, увеличивается потребление кислорода и выделение углекислого газа. Можно вызвать условнорефлекторные изменения обмена веществ, энергетических и тепловых процессов у людей и на словесный раздражитель.
Влияние нервной системы на обменные и энергетические процессы в организме опосредуется несколькими путями:
1) непосредственное влияние нервной системы (через гипоталамус, эфферентные нервы) на ткани и органы;
2) опосредованное влияние нервной системы через гипофиз и его соматотропный гормон;
3) опосредованное влияние нервной системы через тропные гормоны гипофиза и периферические железы внутренней секреции;
4) прямое влияние нервной системы (гипоталамус) на активность желез внутренней секреции и через них на обменные процессы в тканях и органах.
Основным отделом центральной нервной системы, который регулирует все виды обменных и энергетических процессов, является гипоталамус. В гипоталамусе обнаружены группы ядер, которые регулируют обмен углеводов, жиров, белков, воды и солей, а также обмен тепла и потребление пищи.
Как уже указывалось, выраженное влияние на обменные процессы и теплообразование оказывают железы внутренней секреции. Так, гормоны щитовидной железы в определенных дозах, соматотропный гормон гипофиза, инсулин, половые гормоны (андрогены) усиливают синтетические процессы в организме, особенно в отношении белка (анаболическое действие гормонов). Гормоны коры надпочечников и щитовидной железы в больших количествах усиливают катаболизм, т. е. распад белков.
В организме ярко проявляется тесное взаимосвязанное влияние нервной и эндокринной систем на обменные и энергетические процессы. Так, возбуждение симпатической нервной системы не только оказывает прямое стимулирующее действие на обменные процессы, но при этом увеличивается также выход гормонов щитовидной железы и надпочечников (тироксин и адреналин) в кровь. За счет этого дополнительно усиливается обмен веществ и энергии. Кроме того, эти гормоны сами повышают тонус симпатического отдела нервной системы. Значительные изменения в метаболизме и теплообмене происходят при недостатке в организме гормонов желез внутренней секреции. Так, недостаток тироксина приводит к снижению основного обмена. Это связано с уменьшением потребления кислорода тканями и ослаблением теплообразования. В результате снижается температура тела.
Гормоны желез внутренней секреции участвуют в регуляции обмена веществ и энергии, изменяя проницаемость клеточных мембран (инсулин), активируя ферментные системы организма (адреналин, глюкагон и др.) и влияя на их биосинтез (глюкокортикоиды).
Таким образом, регуляция обмена веществ и энергии осуществляется нервной и эндокринной системами, которые обеспечивают приспособление организма к меняющимся условиям его обитания.
Синдром тиреотоксикоза: причины, диагностика, лечение
Тиреотоксикоз — синдром, который встречается при различных патологических состояниях организма человека. Частота тиреотоксикоза по странам Европы и России составляет 1,2%
Тиреотоксикоз — синдром, который встречается при различных патологических состояниях организма человека. Частота тиреотоксикоза по странам Европы и России составляет 1,2% (Фадеев В. В., 2004). Но проблема тиреотоксикоза определяется не столько его распространенностью, сколько тяжестью последствий: влияя на обменные процессы, он ведет к развитию тяжелых изменений во многих системах организма (сердечно-сосудистой, нервной, пищеварительной, репродуктивной и др.).
Синдром тиреотоксикоза, заключающийся в избыточном действии гормонов тироксина и трийодтиронина (T4 и T3) на органы-мишени, в большинстве клинических случаев является следствием патологии щитовидной железы.
Щитовидная железа располагается на передней поверхности шеи, прикрывая спереди и по бокам верхние кольца трахеи. Будучи подковообразной формы, она состоит из двух боковых долей, соединенных перешейком. Закладка щитовидной железы происходит на 3–5 неделе эмбрионального развития, а с 10–12 недели она приобретает способность захватывать йод. Являясь самой крупной эндокринной железой в организме, она вырабатывает тиреоидные гормоны (ТГ) и кальцитонин. Морфофункциональной единицей щитовидной железы является фолликул, стенка которого образована одним слоем эпителиальных клеток — тиреоцитов, а в просвете содержится их секреторный продукт — коллоид.
Тиреоциты захватывают из крови анионы йода и, присоединяя его к тирозину, выводят полученные соединения в виде три- и тетрайодтиронинов в просвет фолликула. Большая часть трийодтиронина образуется не в самой щитовидной железе, а в других органах и тканях, путем отщепления атома йода от тироксина. Оставшаяся после отщепления часть йода вновь улавливается щитовидной железой для участия в синтезе гормонов.
Регуляция функции щитовидной железы находится под контролем гипоталамуса, вырабатывающего тиреотропин-рилизинг-фактор (тиреолиберин), под влиянием которого происходит выброс тиреотропного гормона гипофиза (ТТГ), стимулирующего выработку щитовидной железой Т3 и Т4. Между уровнем тиреоидных гормонов в крови и ТТГ существует отрицательная обратная связь, за счет которой поддерживается их оптимальная концентрация в крови.
Роль тиреоидных гормонов:
Причины тиреотоксикоза
Избыток тиреоидных гормонов в крови может быть следствием заболеваний, проявляющихся гиперфункцией щитовидной железы либо ее разрушением — в этом случае тиреотоксикоз обусловлен пассивным поступлением T4 и T3 в кровь. Кроме того, могут быть и не зависимые от щитовидной железы причины — передозировка тиреоидных гормонов, T4- и T3-секретирующая тератома яичника, метастазы рака щитовидной железы (табл. 1).
Гиперфункция щитовидной железы. Первое место среди заболеваний, сопровождающихся повышенным образованием и секрецией тиреоидных гормонов, занимают диффузный токсический зоб и многоузловой токсический зоб.
Диффузный токсический зоб (ДТЗ) (болезнь Базедова–Грейвса, болезнь Пари) — системное аутоиммунное заболевание с наследственной предрасположенностью, в основе которого лежит выработка стимулирующих аутоантител к рецепторам ТТГ, расположенным на тиреоцитах. О генетической предрасположенности свидетельствует выявление циркулирующих аутоантител у 50% родственников ДТЗ, частое обнаружение у больных гаплотипа HLA DR3, нередкое сочетание с другими аутоиммунными заболеваниями. Сочетание ДТЗ с аутоиммунной хронической надпочечниковой недостаточностью, сахарным диабетом 1-го типа, а также другими аутоиммунными эндокринопатиями обозначается как аутоиммунный полигландулярный синдром 2-го типа. Примечательно, что женщины болеют в 5–10 раз чаще мужчин, манифестация заболевания приходится на молодой и средний возраст. Наследственная предрасположенность при действии триггерных факторов (вирусная инфекция, стрессы и т. д.) ведет к появлению в организме тиреоидстимулирующих иммуноглобулинов — LATS-факторов (long action thyreoid stimulator, длительно действующий тиреоидный стимулятор). Вступая во взаимодействие с рецепторами к тиреотропному гормону на тиреоцитах, тиреоидстимулирующие антитела вызывают увеличение синтеза гормонов T4 и T3, что и приводит к возникновению состояния тиреотоксикоза [2].
Многоузловой токсический зоб — развивается при длительном хроническом недостатке йода в пище. По сути, это одно из звеньев в цепочке последовательных патологических состояний щитовидной железы, формирующихся в условиях йодного дефицита легкой и средней степени тяжести. Диффузный нетоксический зоб (ДНЗ) переходит в узловой (многоузловой) нетоксический зоб, затем развивается функциональная автономия щитовидной железы, являющаяся патофизиологической основой многоузлового токсического зоба. В условиях йодного дефицита щитовидная железа подвергается стимулирующему воздействию ТТГ и местных ростовых факторов, вызывающих гипертрофию и гиперплазию фолликулярных клеток щитовидной железы, что приводит к формированию струмы (стадия ДНЗ). Основой для развития узлов в щитовидной железе является микрогетерогенность тиреоцитов — различная функциональная и пролиферативная активность клеток щитовидной железы.
Если йодный дефицит сохраняется на протяжении многих лет, то стимуляция щитовидной железы, становясь хронической, вызывает гиперплазию и гипертрофию в тиреоцитах, обладающих наиболее выраженной пролиферативной активностью. Что и приводит со временем к возникновению очаговых скоплений тиреоцитов с той же высокой чувствительностью к стимулирующим воздействиям. В условиях продолжающейся хронической гиперстимуляции активное деление тиреоцитов и запаздывание на этом фоне репаративных процессов ведет к развитию активирующих мутаций в генетическом аппарате тиреоцитов, приводящих к автономному их функционированию. Со временем деятельность автономных тиреоцитов приводит к снижению уровня ТТГ и повышению содержания Т3 и Т4 (фаза клинически явного тиреотоксикоза). Так как процесс формирования функциональной автономии щитовидной железы растянут во времени, йодиндуцированный тиреотоксикоз проявляется в старших возрастных группах — после 50 лет [3, 4].
Тиреотоксикоз при беременности. Частота тиреотоксикоза у беременных достигает 0,1%. Основная его причина — диффузный токсический зоб. Так как тиреотоксикоз снижает фертильность, у беременных редко наблюдается тяжелая форма болезни. Нередко беременность наступает во время или после медикаментозного лечения тиреотоксикоза (поскольку это лечение восстанавливает фертильность). Чтобы избежать нежелательной беременности, молодым женщинам с тиреотоксикозом, получающим тионамиды, рекомендуется применять противозачаточные средства.
Токсическая аденома щитовидной железы (болезнь Пламмера) — доброкачественная опухоль щитовидной железы, развивающаяся из фолликулярного аппарата, автономно гиперпродуцирующая тиреоидные гормоны. Токсическая аденома может возникать в ранее существовавшем нетоксическом узле, в связи с этим узловой эутиреоидный зоб рассматривается как фактор риска развития токсической аденомы. В основе патогенеза заболевания лежит автономная гиперпродукция тиреоидных гормонов аденомой, которая не регулируется тиреотропным гормоном. Аденома секретирует в большом количестве преимущественно трийодтиронин, что приводит к подавлению продукции тиреотропного гормона. При этом снижается активность остальной ткани щитовидной железы, окружающей аденому.
ТТГ-секретирующие аденомы гипофиза встречаются редко; на их долю приходится менее 1% всех опухолей гипофиза. В типичных случаях развивается тиреотоксикоз на фоне нормального или повышенного уровня ТТГ.
Избирательная резистентность гипофиза к тиреоидным гормонам — состояние, при котором отсутствует отрицательная обратная связь между уровнем тиреоидных гормонов щитовидной железы и уровнем ТТГ гипофиза, характеризуется нормальным уровнем ТТГ, значительным повышением уровней Т4 и Т3 и тиреотоксикозом (поскольку чувствительность других тканей-мишеней к тиреоидным гормонам не нарушена). Опухоль гипофиза у таких больных не визуализируется.
Пузырный занос и хориокарцинома секретируют большие количества хорионического гонадотропина (ХГ). Хорионический гонадотропин, сходный по своей структуре с ТТГ, вызывает транзиторное подавление тиреотропной активности аденогипофиза и увеличение уровня свободного Т4. Этот гормон — слабый стимулятор рецепторов ТТГ на тиреоцитах. Когда концентрация ХГ превышает 300 000 ед/л (что в несколько раз больше максимальной концентрации ХГ при нормальной беременности), может возникнуть тиреотоксикоз. Удаление пузырного заноса или химиотерапия хориокарциномы устраняют тиреотоксикоз. Уровень ХГ может значительно повышаться и при токсикозе беременных и служить причиной тиреотоксикоза [1].
Разрушение щитовидной железы
Деструкция тиреоцитов, при которой происходит поступление тиреоидных гормонов в кровь и как следствие — развитие тиреотоксикоза, сопровождают воспалительные заболевания щитовидной железы — тиреоидиты. В основном это транзиторные аутоиммунные тиреоидиты (АИТ), к которым относятся безболевой («молчащий») АИТ, послеродовой АИТ, цитокин-индуцированный АИТ. При всех этих вариантах в щитовидной железе происходят пофазовые изменения, связанные с аутоиммунной агрессией: при наиболее типичном течении фаза деструктивного тиреотоксикоза сменяется фазой транзиторного гипотиреоза, после чего в большинстве случаев происходит восстановление функции щитовидной железы.
Послеродовой тиреоидит возникает на фоне избыточной реактивации иммунной системы после естественной гестационной иммуносупрессии (феномен рикошета). Безболевая («молчащая») форма тиреоидита проходит так же, как и послеродовая, но только провоцирующий фактор неизвестен, протекает вне связи с беременностью. Цитокин-индуцированный тиреоидит развивается после назначения по поводу различных заболеваний препаратов интереферона [2].
Развитие тиреотоксикоза возможно не только при аутоиммунном воспалении в щитовидной железе, но и при инфекционном ее повреждении, когда разивается подострый гранулематозный тиреоидит. Считается, что причиной подострого гранулематозного тиреоидита является вирусная инфекция. Предполагают, что возбудителями могут быть вирус Коксаки, аденовирусы, вирус эпидемического паротита, ECHO-вирусы, вирусы гриппа и вирус Эпштейна–Барр. Существует генетическая предрасположенность к подострому гранулематозному тиреоидиту, поскольку заболеваемость выше у лиц с антигеном HLA-Bw35. Для продромального периода (продолжается несколько недель) характерны миалгия, субфебрильная температура, общее плохое самочувствие, ларингит, иногда дисфагия. Синдром тиреотоксикоза возникает у 50% больных и появляется в стадии выраженных клинических проявлений, к которым относится боль на одной стороне передней поверхности шеи, обычно иррадиирующая в ухо или нижнюю челюсть с той же стороны.
Другие причины тиреотоксикоза
Медикаментозный тиреотоксикоз — частая причина тиреотоксикоза. Нередко врач назначает чрезмерные дозы гормонов; в других случаях больные тайком принимают излишние количества гормонов, иногда с целью похудеть.
T4— и T3-секретирующая тератома яичника (яичниковая струма) и крупные гормонально-активные метастазы фолликулярного рака щитовидной железы — очень редкие причины тиреотоксикоза.
Клиническая картина при синдроме тиреотоксикоза
Сердечно-сосудистая система. Наиболее важным органом-мишенью при нарушениях функции щитовидной железы является сердце. В 1899 г. R. Kraus ввел термин «тиреотоксическое сердце», под которым понимается симптомокомплекс нарушений деятельности сердечно-сосудистой системы, вызванных токсическим действием избытка тиреоидных гормонов, характеризующимся развитием гиперфункции, гипертрофии, дистрофии, кардиосклероза и сердечной недостаточности.
Патогенез сердечно-сосудистых нарушений при тиреотоксикозе связан со способностью ТГ непосредственно связываться с кардиомиоцитами, оказывая положительный инотропный эффект. Кроме того, повышая чувствительность и экспрессию адренорецепторов, тиреоидные гормоны обуславливают значительные изменения гемодинамики и развитие острой патологии сердца, особенно у больных с ишемической болезнью сердца. Происходит увеличение ЧСС, повышение ударного объема (УО) и минутного объема (МО), ускорение кровотока, снижение общего и периферического сопротивления сосудов (ОПСС), изменение артериального давления. Систолическое давление умеренно нарастает, диастолическое остается нормальным или пониженным, вследствие чего увеличивается пульсовое давление. Помимо всего перечисленного тиреотоксикоз сопровождается увеличением объема циркулирующей крови (ОЦК) и эритроцитарной массы. Причиной увеличения ОЦК является изменение сывороточного уровня эритропоэтина в соответствии с изменением сывороточного уровня тироксина, что приводит к увеличению массы эритроцитов. В результате увеличения минутного объема и массы циркулирующей крови, с одной стороны, и снижения периферического сопротивления, с другой, увеличиваются пульсовое давление и нагрузка на сердце в диастолу.
Основными клиническими проявлениями патологии сердца при тиреотоксикозе являются синусовая тахикардия, мерцание предсердий (МП), сердечная недостаточность и метаболическая форма стенокардии. В случае наличия у пациента ишемической болезни сердца (ИБС), гипертонической болезни, пороков сердца тиреотоксикоз лишь ускорит возникновение аритмий. Существует прямая зависимость МП от степени тяжести и длительности заболевания.
Основной особенностью синусовой тахикардии является то, что она не исчезает во время сна и незначительная физическая нагрузка резко увеличивает частоту сердечных сокращений. В редких случаях встречается синусовая брадикардия. Это может быть связано с врожденными изменениями либо с истощением функции синусового узла с развитием синдрома его слабости.
Мерцание предсердий встречается в 10–22% случаев, причем частота этой патологии увеличивается с возрастом. В начале заболевания мерцание предсердий носит пароксизмальный характер, а с прогрессированием тиреотоксикоза может перейти в постоянную форму. У больных молодого возраста без сопутствующей сердечно-сосудистой патологии после субтотальной резекции щитовидной железы или успешной тиреостатической терапии происходит восстановление синусового ритма. В патогенезе мерцания предсердий важную роль играет нарушение электролитного баланса, точнее, снижение уровня внутриклеточного калия в миокарде, а также истощение номотропной функции синусового узла, что приводит к его истощению и переходу на патологический ритм.
Для тиреотоксикоза более характерны предсердные нарушения ритма, а появление желудочковых аритмий характерно лишь для тяжелой формы. Это может быть связано с более высокой чувствительностью предсердий к аритмогенному действию ТТГ по сравнению с желудочками, так как плотность бета-адренорецепторов в ткани предсердий преобладает. Как правило, желудочковые аритмии встречаются при сочетании тиреотоксикоза с сердечно-сосудистыми заболеваниями. При наступлении стойкого эутиреоза они сохраняются [5].
Опорно-двигательный аппарат. Усиление катаболизма приводит к слабости и атрофии мышц (тиреотоксическая миопатия). Больные выглядят истощенными. Мышечная слабость проявляется при ходьбе, подъеме в гору, вставании с колен или поднятии тяжестей. В редких случаях встречается преходящий тиреотоксический паралич, длящийся от нескольких минут до нескольких суток.
Повышенный уровень тиреоидных гормонов приводит к отрицательному минеральному балансу с потерей кальция, что проявляется усиленной резорбцией кости и сниженным кишечным всасыванием этого минерала. Резорбция костной ткани преобладает над ее образованием, поэтому концентрация кальция в моче повышена.
У больных гипертиреозом обнаруживаются низкие уровни метаболита витамина D-1,25(ОН)2D, иногда гиперкальциемия и снижение уровня паратгормона в сыворотке. Клинически все эти нарушения приводят к развитию диффузного остеопороза. Возможны боли в костях, патологические переломы, коллапс позвонков, формирование кифоза. Артропатия при тиреотоксикозе развивается редко, по типу гипертрофической остеоартропатии с утолщением фаланг пальцев и периостальными реакциями.
Нервная система. Поражение нервной системы при тиреотоксикозе возникает практически всегда, поэтому раньше его называли «нейротиреозом» или «тиреоневрозом». В патологический процесс вовлекаются центральная нервная система, периферические нервы и мышцы.
Воздействие избытка тиреоидных гормонов в первую очередь приводит к развитию симптоматики неврастенического характера. Типичны жалобы на повышенную возбудимость, беспокойство, раздражительность, навязчивые страхи, бессонницу, отмечается изменение поведения — суетливость, плаксивость, избыточная моторная активность, потеря способности концентрировать внимание (больной резко переключается с одной мысли на другую), эмоциональная неустойчивость с быстрой сменой настроения от ажитации до депрессии. Истинные психозы редки. Синдром заторможенности и депрессии, названный «апатичным тиреотоксикозом», обычно возникает у пожилых больных.
Фобические проявления весьма характерны для тиреотоксикоза. Часто возникает кардиофобия, клаустрофобия, социофобия.
В ответ на физическую и эмоциональную нагрузку возникают панические атаки, проявляющиеся резким учащением пульса, повышением артериального давления, побледнением кожи, сухостью во рту, ознобоподобным дрожанием, страхом смерти.
Невротические симптомы при тиреотоксикозе неспецифичны, а по мере развития и утяжеления заболевания угасают, сменяясь тяжелыми органными поражениями.
Тремор — ранний симптом тиреотоксикоза. Этот гиперкинез сохраняется и в покое, и при движениях, причем эмоциональная провокация усиливает его выраженность. Тремор захватывает руки (симптом Мари — тремор пальцев вытянутых рук), веки, язык, а иногда и все тело («симптом телеграфного столба»).
По мере утяжеления заболевания прогрессируют быстрая утомляемость, мышечная слабость, диффузное похудение, атрофия мышц. У некоторых больных мышечная слабость достигает крайней степени тяжести и даже приводит к смерти. Исключительно редко при тяжелом тиреотоксикозе могут внезапно возникнуть приступы генерализованной мышечной слабости (периодический тиреотоксический гипокалиемический паралич), захватывающей мышцы туловища и конечностей, в том числе и дыхательные мышцы. В некоторых случаях параличу предшествуют приступы слабости в ногах, парестезии, патологическая утомляемость мышц. Паралич развивается бурно. Такие приступы иногда могут быть единственным проявлением тиреотоксикоза. При электромиографии у больных с периодическим параличом выявляются полифазия, уменьшение потенциалов действия, наличие спонтанной активности мышечных волокон и фасцикуляций.
Хроническая тиреотоксическая миопатия возникает при длительном течении тиреотоксикоза, характеризуется прогрессирующей слабостью и утомляемостью в проксимальных группах мышц конечностей, чаще ног. Отмечаются затруднения при подъеме по лестнице, вставании со стула, расчесывании волос. Постепенно развивается симметричная гипотрофия мышц проксимальных отделов конечностей.
Тиреотоксический экзофтальм. Тиреотоксический экзофтальм встречается всегда на фоне тиреотоксикоза, чаще у женщин. Глазная щель у таких больных распахнута, хотя экзофтальма при этом нет, либо он не превышает 2 мм. Увеличение глазной щели происходит за счет ретракции верхнего века. Могут быть обнаружены и другие симптомы: при взгляде прямо иногда видна полоска склеры между верхним веком и радужкой (симптом Дальримпля). При взгляде вниз опускание верхнего века отстает от движения глазного яблока (симптом Грефе). Эти симптомы обусловлены повышением тонуса гладких мышц, поднимающих верхнее веко. Характерно редкое мигание (симптом Штелльвага), нежный тремор век при их смыкании, но веки смыкаются полностью. Объем движений экстраокулярных мышц не нарушен, глазное дно остается нормальным, функции глаза не страдают. Репозиция глаза не затруднена. Использование инструментальных методов исследования, включая компьютерную томографию и ядерно-магнитный резонанс, доказывает отсутствие изменений в мягких тканях орбиты. Описанные симптомы исчезают на фоне медикаментозной коррекции дисфункции щитовидной железы [6].
Глазные симптомы тиреотоксикоза необходимо отличать от самостоятельного заболевания эндокринной офтальмопатии.
Эндокринная офтальмопатия (Грейвса) — это заболевание связано с поражением периорбитальных тканей аутоиммунного генеза, которое в 95% случаев сочетается с аутоиммунными заболеваниями щитовидной железы. В его основе лежит лимфоцитарная инфильтрация всех образований глазницы и ретроорбитальный отек. Основной симптом офтальмопатии Грейвса — экзофтальм. Отек и фиброз глазодвигательных мышц приводят к ограничению подвижности глазного яблока и диплопии. Больные жалуются на резь в глазах, светобоязнь, слезотечение. Из-за несмыкания век роговица высыхает и может изъязвляться. Сдавление зрительного нерва и кератит могут привести к слепоте.
Пищеварительная система. Потребление пищи увеличивается, у некоторых больных возникает неутолимый аппетит. Несмотря на это, больные обычно худые. Из-за усиления перистальтики стул частый, но понос бывает редко.
Половая система. Тиреотоксикоз у женщин снижает фертильность и может вызвать олигоменорею. У мужчин подавляется сперматогенез, изредка снижается потенция. Иногда отмечается гинекомастия, обусловленная ускоренным периферическим превращением андрогенов в эстрогены (несмотря на высокий уровень тестостерона). Тиреоидные гормоны увеличивают концентрацию глобулина, связывающего половые гормоны, и тем самым повышают общее содержание тестостерона и эстрадиола; в то же время уровни лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) в сыворотке могут быть как повышенными, так и нормальными.
Обмен веществ. Больные обычно худые. Для пожилых характерна анорексия. Напротив, у некоторых молодых больных аппетит повышен, поэтому они прибавляют в весе. Поскольку тиреоидные гормоны усиливают теплопродукцию, усиливается и теплоотдача за счет потоотделения, что приводит к легкой полидипсии. Многие плохо переносят тепло. У больных с инсулинозависимым сахарным диабетом при тиреотоксикозе возрастает потребность в инсулине.
Щитовидная железа обычно увеличена. Размеры и консистенция зоба зависят от причины тиреотоксикоза. В гиперфункционирующей железе усиливается кровоток, что обуславливает появление местного сосудистого шума.
Тиреотоксический криз представляет собой резкое обострение всех симптомов тиреотоксикоза, являясь тяжелым осложнением основного заболевания, сопровождающегося гиперфункцией щитовидной железы (в клинической практике это, как правило, токсический зоб). Развитию криза способствуют следующие факторы:
Патогенез криза заключается в чрезмерном поступлении в кровь тиреоидных гормонов и тяжелом токсическом поражении сердечно-сосудистой системы, печени, нервной системы и надпочечников. В клинической картине характерно резкое возбуждение (вплоть до психоза с бредом и галлюцинациями), которое затем сменяется адинамией, сонливостью, мышечной слабостью, апатией. При осмотре: лицо резко гиперемировано; глаза широко раскрыты (выраженный экзофтальм), мигание редкое; профузная потливость, в дальнейшем сменяющаяся сухостью кожи вследствие выраженного обезвоживания; кожа горячая, гиперемированная; высокая температура тела (до 41–42 °C).
Высокое систолическое артериальное давление (АД), диастолическое АД значительно снижено, при далеко зашедшем кризе систолическое АД резко снижается, возможно развитие острой сердечно-сосудистой недостаточности; тахикардия до 200 ударов в минуту переходит в мерцание предсердий; усиливаются диспептические расстройства: жажда, тошнота, рвота, жидкий стул. Возможны увеличение печени и развитие желтухи. Дальнейшее прогрессирование криза ведет к потере ориентации, симптомам острой надпочечниковой недостаточности. Клинические симптомы криза чаще нарастают в течение нескольких часов. В крови ТТГ может не определяться, уровень же T4 и T3 очень высокий. Наблюдается гипергликемия, возрастают значения мочевины, азота, изменяется кислотно-основное состояние и электролитный состав крови — уровень калия повышен, натрия — падает. Характерен лейкоцитоз с нейтрофильным сдвигом влево.
Диагностика
При подозрении на тиреотоксикоз обследование включает два этапа: оценку функции щитовидной железы и выяснение причины повышения тиреоидных гормонов.
Оценка функции щитовидной железы
1. Общий T4 и свободный T4 повышены почти у всех больных с тиреотоксикозом.
2. Общий T3 и свободный T3 также повышены. Менее чем у 5% больных повышен только общий T3, тогда как общий T4 остается нормальным; такие состояния называют T3-тиреотоксикозом.
3. Базальный уровень ТТГ сильно снижен, либо ТТГ не определяется. Проба с тиреолиберином необязательна. Базальный уровень ТТГ снижен у 2% пожилых людей с эутиреозом. Нормальный или увеличенный базальный уровень ТТГ на фоне повышенных уровней общего T4 или общего T3 указывает на тиреотоксикоз, вызванный избытком ТТГ.
4. Тиреоглобулин. Повышение уровня тиреоглобулина в сыворотке крови выявляется при различных формах тиреотоксикоза: диффузном токсическом зобе, подостром и аутоиммунном тиреоидите, многоузловом токсическом и нетоксическом зобе, эндемическом зобе, раке щитовидной железы и его метастазах. Для медуллярного рака щитовидной железы характерно нормальное или даже сниженное содержание тиреоглобулина в сыворотке крови. При тиреоидитах концентрация тиреоглобулина в сыворотке крови может не соответствовать степени клинических симптомов тиреотоксикоза.
Современные лабораторные методы позволяют диагностировать два варианта тиреотоксикоза, которые очень часто являются стадиями одного процесса:
5. Поглощение радиоактивного йода (I123 или I131) щитовидной железой. Для оценки функции щитовидной железы важен тест на поглощение небольшой дозы радиоактивного йода в течение 24 ч. Спустя 24 часа после приема внутрь дозы I123 или I131 измеряется захват изотопа щитовидной железой и затем выражается в процентном соотношении. Необходимо учитывать, что поглощение радиоактивного йода существенно зависит от содержания йода в пище и в окружающей среде.
Состояние йодного пула пациента по-разному отражается на результатах измерения поглощения радиоактивного йода при различных заболеваниях щитовидной железы. Гипертироксинемия с высоким захватом радиоактивного йода характерна для токсического зоба. Причин для гипертироксинемии на фоне низкой величины захвата радиоактивного йода множество: избыток йода в организме, тиреоидит, прием тиреоидного гормона, эктопическая выработка тиреоидного гормона. Поэтому при обнаружении высокого содержания тиреоидных гормонов в крови на фоне низкого захвата I123 или I131 необходимо провести дифференциальную диагностику заболеваний (табл. 2) [7].
6. Радионуклидное сканирование. Функциональное состояние щитовидной железы можно определить в тесте с захватом радиофармпрепарата (радиоактивного йода или технеция пертехнетата). При использовании изотопа йода области железы, которые захватывают йод, видны на сцинтиграмме. Нефункционирующие области не визуализируются и называются «холодными».
7. Супрессивные пробы с T3 или T4. При тиреотоксикозе поглощение радиоактивного йода щитовидной железой под влиянием экзогенных тиреоидных гормонов (3 мг левотироксина однократно внутрь либо по 75 мкг/сут лиотиронина внутрь в течение 8 сут) не уменьшается. В последнее время эту пробу используют редко, поскольку разработаны высокочувствительные методы определения ТТГ и методы сцинтиграфии щитовидной железы. Проба противопоказана при заболеваниях сердца и пожилым больным.
8. Ультразвуковое исследование (УЗИ), или эхография, или ультрасонография. Этот метод информативен и значительно помогает в диагностике аутоиммунного тиреоидита, в меньшей степени — диффузного токсического зоба.
Установление причины тиреотоксикоза
Дифференциальная диагностика заболеваний, сопровождающихся тиреотоксикозом
Из всех причин, ведущих к развитию тиреотоксикоза, наиболее актуальными (в силу своей распространенности) являются диффузный токсический зоб и многоузловой токсический зоб. Очень часто причиной неудачного лечения токсического зоба являются как раз ошибки в дифференциальной диагностике болезни Грейвса и многоузлового токсического зоба, ввиду того, что методы лечения этих двух заболеваний различаются. Поэтому, в том случае, если наличие у пациента тиреотоксикоза было подтверждено при гормональном исследовании, в большинстве случаев приходится дифференцировать болезнь Грейвса и функциональную автономию щитовидной железы (узловой и многоузловой токсический зоб).
При обоих вариантах токсического зоба клиника в первую очередь определяется синдромом тиреотоксикоза. При проведении дифференциального диагноза необходимо учитывать возрастную особенность: у молодых людей, у которых, как правило, речь идет о болезни Грейвса, в большинстве случаев имеет место развернутая классическая клиническая картина тиреотоксикоза, тогда как у пожилых пациентов, у которых в нашем регионе чаще встречается многоузловой токсический зоб, нередко имеет место олиго- и даже моносимптомное течение тиреотоксикоза. Например, единственным его проявлением могут быть суправентрикулярные аритмии, которые долго связываются с ИБС, или необъяснимый субфебрилитет. В большинстве случаев уже по данным анамнеза, осмотра и клинической картины возможно поставить правильный диагноз. Молодой возраст пациента, относительно короткий анамнез заболевания (до года), диффузное увеличение щитовидной железы и выраженная эндокринная офтальмопатия — характерные признаки болезни Грейвса. В противоположность этому пациенты с многоузловым токсическим зобом могут указывать на то, что много лет или даже десятилетий назад у них обнаруживался узловой или диффузный зоб без нарушения функции щитовидной железы.
Сцинтиграфия щитовидной железы: для болезни Грейвса характерно диффузное повышение захвата радиофармпрепарата, при функциональной автономии выявляются «горячие» узлы либо чередование зон повышенного и пониженного накопления. Нередко оказывается, что в многоузловом зобе наиболее крупные узлы, выявленные при УЗИ, по данным сцинтиграфии оказываются «холодными» или «теплыми», а тиреотоксикоз развивается в результате гиперфункционирования ткани, окружающей узлы.
Дифференциальная диагностика токсического зоба и тиреоидитов не вызывает особых затруднений. При подостром гранулематозном тиреоидите ведущими симтомами являются: недомогание, лихорадка, боль в области щитовидной железы. Боль иррадиирует в уши, при глотании или поворотах головы усиливается. Щитовидная железа при пальпации чрезвычайно болезненная, очень плотная, узловатая. Воспалительный процесс обычно начинается в одной из долей щитовидной железы и постепенно захватывает другую долю. Скорость оседания эритроцитов (СОЭ) повышена, антитиреоидные аутоантитела, как правило, не выявляются, поглощение радиоактивного йода щитовидной железой резко снижено.
Транзиторные аутоиммунные тиреоидиты (подострые лимфоцитарные тиреоидиты) — выяснение в анамнезе родов, аборта, употребления препаратов интерферона. Тиреотоксическая (начальная) стадия подострого послеродового тиреоидита продолжается 4–12 недель, сменяясь гипотиреоидной стадией длительностью несколько месяцев. Сцинтиграфия щитовидной железы: для тиреотоксической стадии всех трех видов транзиторных тиреоидитов характерно снижение накопления радиофармпрепарата. Ультразвуковое исследование выявляет снижение эхогенности паренхимы.
Острый психоз. Вообще психоз — это болезненное расстройство психики, проявляющееся целиком или преимущественно неадекватным отражением реального мира с нарушением поведения, изменением различных сторон психической деятельности, обычно с возникновением не свойственных нормальной психике явлений (галлюцинации, бред, психомоторные, аффективные расстройства и др.). Токсическое действие тиреоидных гормонов способно вызвать острый симптоматический психоз (т. е. как одно из проявлений общего неинфекционного заболевания, инфекции и интоксикации). Почти у трети больных, госпитализированных с острым психозом, общий T4 и свободный T4 повышены. У половины больных с повышенным уровнем T4 увеличен и уровень T3. Через 1–2 нед эти показатели нормализуются без лечения антитиреоидными средствами. Предполагают, что увеличение уровней тиреоидных гормонов вызвано выбросом ТТГ. Однако уровень ТТГ при первичном обследовании госпитализированных больных с психозом обычно снижен или находится на нижней границе нормы. Вероятно, уровень ТТГ может повышаться на ранней стадии психоза (до госпитализации). Действительно, у некоторых больных с пристрастием к амфетаминам, госпитализированных с острым психозом, находят недостаточное снижение уровня ТТГ на фоне повышенного уровня T4.
Лечение при синдроме тиреотоксикоза
Лечение тиреотоксикоза зависит от причин, его вызвавших.
Токсический зоб
Методы лечения болезни Грейвса и различных клинических вариантов функциональной автономии щитовидной железы отличаются. Главное отличие заключается в том, что в случае функциональной автономии щитовидной железы на фоне тиреостатической терапии невозможно достижение стойкой ремиссии тиреотоксикоза; после отмены тиреостатиков он закономерно развивается вновь. Таким образом, лечение функциональной автономии заключается в хирургическом удалении щитовидной железы или ее деструкции при помощи радиоактивного йода-131. Это связано с тем, что тиреостатической терапией полной ремиссии тиреотоксикоза добиться не удается, после отмены препарата все симптомы возвращаются. В случае болезни Грейвса у отдельных групп пациентов возможна стойкая ремиссия при проведении консервативной терапии.
Длительную (18–24 месяца) тиреостатическую терапию, как базовый метод лечения болезни Грейвса, можно планировать только у пациентов с небольшим увеличением щитовидной железы, при отсутствии в ней клинически значимых узловых образований. В случае развития рецидива после одного курса тиреостатической терапии назначение второго курса бесперспективно.
Тиреостатическая терапия
Тиамазол (Тирозол®). Антитиреоидный препарат, нарушающий синтез гормонов щитовидной железы за счет блокирования пероксидазы, участвующей в йодировании тирозина, снижает внутреннюю секрецию Т4. В нашей стране и в странах Европы наиболее популярны препараты тиамазола. Тиамазол снижает основной обмен, ускоряет выведение из щитовидной железы йодидов, повышает реципрокную активацию синтеза и выделения гипофизом ТТГ, что сопровождается некоторой гиперплазией щитовидной железы. Он не влияет на тиреотоксикоз, развившийся вследствие высвобождения гормонов после разрушения клеток щитовидной железы (при тиреоидите).
Продолжительность действия однократно принятой дозы Тирозола® составляет почти 24 часа, поэтому всю суточную дозу назначают в один прием или разделяют на две-три разовые дозы. Тирозол® представлен в двух дозировках — 10 мг и 5 мг тиамазола в одной таблетке. Дозировка Тирозола® 10 мг позволяет уменьшить в два раза количество таблеток, принимаемых пациентом, и, соответственно, повысить уровень комплаентности пациента.
Пропилтиоурацил. Блокирует тиреоидную пероксидазу и угнетает превращение ионизированного йода в активную форму (элементарный йод). Нарушает йодирование тирозиновых остатков молекулы тиреоглобулина с образованием моно- и дийодтирозина и, далее, три- и тетрайодтиронина (тироксина). Экстратиреоидное действие заключается в торможении периферической трансформации тетрайодтиронина в трийодтиронин. Устраняет или ослабляет тиреотоксикоз. Обладает зобогенным эффектом (увеличение размеров щитовидной железы), обусловленным повышением секреции тиреотропного гормона гипофиза в ответ на понижение концентрации гормонов щитовидной железы в крови. Средняя суточная дозировка пропилтиоурацила составляет 300–600 мг/сут. Препарат принимают дробно, каждые 8 часов. ПТУ накапливается в щитовидной железе. Показано, что дробный прием ПТУ гораздо эффективнее однократного приема всей суточной дозы. ПТУ обладает менее продолжительным действием, чем тиамазол.
Для длительной терапии болезни Грейвса наиболее часто используется схема «блокируй и замещай» (антитиреоидный препарат блокирует активность щитовидной железы, левотироксин предупреждает развитие гипотиреоза). Она не имеет преимуществ перед монотерапией тиамазолом в плане частоты развития рецидивов, но за счет использования больших доз тиростатика позволяет более надежно поддерживать эутиреоз; в случае монотерапии дозу препарата очень часто приходится изменять то в одну, то в другую сторону.
При тиреотоксикозе средней тяжести сначала обычно назначается около 30 мг тиамазола (Тирозол®). На этом фоне (примерно через 4 недели) в большинстве случаев удается достигнуть эутиреоз, о чем будет свидетельствовать нормализация уровня свободного T4 крови (уровень ТТГ еще долго будет оставаться низким). Начиная с этого момента, доза тиамазола постепенно снижается до поддерживающей (10–15 мг) и к лечению добавляется левотироксин (Эутирокс®) в дозе 50–75 мкг в сутки. Указанную терапию под периодическим контролем уровня ТТГ и свободного Т4 пациент получает 18–24 месяца, после чего она отменяется. В случае развития рецидива после курса тиростатической терапии пациенту показано радикальное лечение: оперативное вмешательство или терапия радиоактивным йодом.
Бета-адреноблокаторы
Пропранолол быстро улучшает состояние больных, блокируя бета-адренорецепторы. Пропранолол несколько снижает и уровень T3, тормозя периферическое превращение T4 в T3. Этот эффект пропранолола, по-видимому, не опосредуется блокадой бета-адренорецепторов. Обычная доза пропранолола — 20–40 мг внутрь каждые 4–8 ч. Дозу подбирают так, чтобы снизить ЧСС в покое до 70–90 мин–1. По мере исчезновения симптомов тиреотоксикоза дозу пропранолола уменьшают, а по достижении эутиреоза препарат отменяют.
Бета-адреноблокаторы устраняют тахикардию, потливость, тремор и тревожность. Поэтому прием бета-адреноблокаторов затрудняет диагностику тиреотоксикоза.
Другие бета-адреноблокаторы не более эффективны, чем пропранолол. Селективные бета1-адреноблокаторы (метопролол) не снижают уровень T3.
Бета-адреноблокаторы особенно показаны при тахикардии даже на фоне сердечной недостаточности при условии, что тахикардия обусловлена тиреотоксикозом, а сердечная недостаточность — тахикардией. Относительное противопоказание к применению пропранолола — хроническая обструктивная болезнь легких.
Йодиды
Насыщенный раствор калия йодида в дозе 250 мг 2 раза в сутки оказывает лечебное действие у большинства больных, но примерно через 10 сут лечение обычно становится неэффективным (феномен «ускользания»). Калия йодид используют в основном для подготовки больных к операциям на щитовидной железе, так как йод вызывает уплотнение железы и уменьшает ее кровоснабжение. Калия йодид очень редко применяют как средство выбора при длительном лечении тиреотоксикоза.
В настоящее время все больше специалистов во всем мире склоняются к тому, что целью радикального лечения болезни Грейвса является стойкий гипотиреоз, который достигается почти полным оперативным удалением щитовидной железы (предельно субтотальная резекция) или введением достаточных для этого доз I131, после чего пациенту назначается заместительная терапия левотироксином. Крайне нежелательным следствием более экономных резекций щитовидной железы являются многочисленные случаи послеоперационных рецидивов тиреотоксикоза.
В связи с этим важно понимать, что патогенез тиреотоксикоза при болезни Грейвса преимущественно связан не с большим объемом гиперфункционирующей ткани щитовидной железы (она может быть вообще не увеличена), а с циркуляцией стимулирующих щитовидную железу антител, которые продуцируются лимфоцитами. Таким образом, при удалении во время операции по поводу болезни Грейвса не всей щитовидной железы в организме оставляется «мишень» для антител к рецептору ТТГ, которые даже после полного удаления щитовидной железы могут продолжать циркулировать у пациента на протяжении всей жизни. То же самое относится и к лечению болезни Грейвса радиоактивным I131.
Наряду с этим современные препараты левотироксина позволяют поддерживать у пациентов с гипотиреозом качество жизни, которое мало отличается от такового у здоровых людей. Так, препарат левотироксина Эутирокс® представлен в шести самых необходимых дозировках: 25, 50, 75, 100, 125 и 150 мкг левотироксина. Широкий спектр дозировок позволяет упростить подбор необходимой дозы левотироксина и избежать необходимости дробить таблетку для получения необходимой дозировки. Таким образом достигается высокая точность дозирования и, как следствие, оптимальный уровень компенсации гипотиреоза. Также отсутствие необходимости дробить таблетки позволяет повысить комплаентность пациентов и качество их жизни. Это подтверждает не только клиническая практика, но и данные многих исследований, прицельно изучавших этот вопрос.
При условии ежедневного приема заместительной дозы левотироксина для пациента практически отсутствуют какие-либо ограничения; женщины могут планировать беременность и рожать, не опасаясь развития рецидива тиреотоксикоза во время беременности или (достаточно часто) после родов. Очевидно, что в прошлом, когда, собственно, и сложились подходы к лечению болезни Грейвса, подразумевающие более экономные резекции щитовидной железы, гипотиреоз закономерно рассматривался как неблагоприятный исход операции, поскольку терапия экстрактами щитовидной железы животных (тиреоидин) не могла обеспечить должную компенсацию гипотиреоза.
К очевидным преимуществам терапии радиоактивным йодом относятся:
Единственные противопоказания: беременность и грудное вскармливание [4].
Лечение тиреотоксического криза. Начинается с введения тиреостатических препаратов. Начальная доза тиамазола — 30–40 мг per os. При невозможности проглотить препарат — введение через зонд. Эффективным является внутривенное капельное введение 1% раствора Люголя, основанного на йодиде натрия (100–150 капель в 1000 мл 5% раствора глюкозы), либо по 10–15 капель каждые 8 часов внутрь.
Для борьбы с надпочечниковой недостаточностью применяют глюкокортикоидные препараты. Гидрокортизон вводится внутривенно капельно по 50–100 мг 3–4 раза в сутки в сочетании с большими дозами аскорбиновой кислоты. Рекомендовано назначение бета-адреноблокаторов в большой дозе (10–30 мг 4 раза в сутки внутрь) или внутривенно 0,1% раствор пропранолола, начиная с 1,0 мл под контролем пульса и артериального давления. Отменяют их постепенно. Внутрь назначается резерпин 0,1–0,25 мг 3–4 раза в сутки. При выраженных микроциркуляторных нарушениях — Реополиглюкин, Гемодез, Плазма. Для борьбы с дегидратацией назначают 1–2 л 5% раствора глюкозы, физиологические растворы. В капельницу добавляются витамины (С, B1, B2, B6).
Лечение транзиторных аутоиммунных тиреоидитов в тиреотоксическую стадию: назначение тиреостатиков не показано, так как гиперфункции щитовидной железы нет. При выраженной сердечно-сосудистой симптоматике назначают бета-адреноблокаторы.
При беременности никогда не применяют I131, так как он проходит через плаценту, накапливается в щитовидной железе плода (начиная с 10-й недели беременности) и вызывает кретинизм у ребенка.
При беременности препаратом выбора считается пропилтиоурацил, но может использоваться и тиамазол (Тирозол®) в минимально эффективной дозе. Дополнительный прием левотироксина (схема «блокируй и замещай») не показан, т. к. это приводит к увеличению потребности в тиреостатике.
Если необходима субтотальная резекция щитовидной железы, то ее лучше делать в I или во II триместрах, поскольку любые хирургические вмешательства в III триместре могут вызвать преждевременные роды.
При правильном лечении тиреотоксикоза беременность заканчивается рождением здорового ребенка в 80–90% случаев. Частота преждевременных родов и самопроизвольных абортов такая же, как в отсутствие тиреотоксикоза. ЃЎ
Литература
В. В. Смирнов, доктор медицинских наук, профессор
Н. В. Маказан
