Дистонии-плюс dyt12: трудности диагностики в раннем периоде заболевания
*Пятилетний импакт фактор РИНЦ за 2020 г.

Читайте в новом номере
Дистонии представляют собой группу заболеваний различной этиологии, на сегодняшний день разработана этиологическая классификация, подразделяющая все дистонии на первичные (идиопатические) и вторичные.
В данной статье представлен собственный клинический опыт наблюдения и постановки окончательного диагноза у пациента с одним из вариантов течения синдрома генетически детерминированной дистонии-плюс в виде дистонии-паркинсонизма с ранним началом (DYT12) и манифестацией в раннем пубертатном периоде — это аутосомно-доминантное заболевание с генетически доказанной мутацией в гене АТР1А3. Авторы приводят различия данного заболевания и классической дистонии. При данном виде дистонии отмечаются особенности возникновения первых симптомов заболевания, напоминающие нейроинфекционные проявления, нередко триггером ситуации могут послужить различные инфекционные процессы. В статье подробно описаны первые клинические проявления (соматический и неврологический статус) и дальнейшая трансформация симптомов с течением заболевания, данные дополнительных инструментальных методов обследования, таких как нейровизуализация головного мозга, электромиография. Благодаря их использованию авторы смогли заподозрить данное заболевание и в дальнейшем подтвердить диагноз при молекулярно-генетическом обследовании (таргетная панель на нейродегенеративные заболевания).
Ключевые слова: диагностика, клинические проявления, ранние симптомы, дистония-плюс, DYT12, педиатрическая практика.
Для цитирования: Шишкина Е.В., Базилевская Т.Н., Белкина А.Б. и др. Дистонии-плюс dyt12: трудности диагностики в раннем периоде заболевания. РМЖ. 2020;2:37-39.
Dystonia-plus DYT12: difficulties in diagnosis of an early disease onset
1 Krasnoyarsk State Medical University named after Prof. V.F. Voino-Yasenetsky, Krasnoyarsk
2 Krasnoyarsk Trans-Regional Children’s Clinical Hospital No. 1, Krasnoyarsk
Dystonia is a group of diseases of various etiology. To date, there is an etiological classification dividing all dystonia into primary (idiopathic) and secondary variants.
This article presents our own clinical experience concerning follow-up and establishing the final diagnosis in a patient with one of the genetically determined dystonia-plus course variants in the form of early dystonia parkinsonism onset (DYT12) with manifestation in the early puberty period. It is an autosomal dominant disease with a genetically proven ATR1A3 gene mutation. The distinctive patterns of this disease from the classic dystonia view are described in detail. In this dystonia type, there are patterns of the first disease signs that resemble neuroinfection manifestations. Commonly, the trigger of such an event can serve as various infectious processes. The article describes in detail the first clinical manifestations in the somatic and neurological status and further signs transformation over the disease course, data from additional instrumental examinations such as brain imaging, electromyography. Based on these examinations, the authors were able t o initially suspect this disease and later confirm it during molecular genetic examination (target genetic panel for neurodegenerative diseases).
Keywords: diagnosis, clinical manifestations, early signs, DYT12, dystonia-plus, pediatric practice.
For citation: Shishkina E.V., Bazilevskaia T.N., Belkina A.B. et al. Dystonia-plus DYT1: difficulties in diagnosis of an early disease onset.
RMJ. 2020;2:37–39.
Введение
Количество пациентов с нейрогенетическими заболеваниями неуклонно растет с каждым годом, что в большей степени обусловлено не столько увеличением встречаемости данной патологии в общей популяции, сколько быстрым развитием современных методов обследования, включая медико-генетическое консультирование [1, 2]. При этом в настоящее время выявляют редко встречающиеся синдромы, которые в условиях высокой информационной оснащенности специалистов и доступности узкоспециализированных высокотехнологичных методов обследования требуют длительного диагностического поиска [3].
Дистонии представляют собой группу заболеваний различной этиологии, характеризующихся проявлениями в виде непроизвольных движений в сочетании с аномальным положением тела или конечностей [1, 4].
На сегодняшний день разработана этиологическая классификация, подразделяющая все дистонии на первичные (идиопатические: изолированные или сочетающиеся с другими неврологическими проявлениями (паркинсонизм, миоклонусы) формы) и вторичные, обусловленные метаболическими, нейродегенеративными и другими соматическими заболеваниями [5].
Также существует генетическая классификация по этиопатогенетическим характеристикам, включающим причины развития заболевания, характер наследования и особенности их клинической картины [6]. В настоящее время выделено 21 моногенное заболевание, в структуре которых различают первичные дистонии (DYT1, DYT2, DYT4, DYT7, DYT13, DYT17, DYT21), дистонии-плюс (DYT5, DYT11, DYT12, DYT14, DYT15), нейродегенеративные дистонии с паркинсонизмом (DYT3, DYT16) и пароксизмальные дискинезии (DYT8, DYT9, DYT10, DYT18, DYT19, DYT20) [6, 7].
Мутация гена ATP1A3 связана с тремя известными неврологическими синдромами: дистония-паркинсонизм с быстрым началом (RDP); перемежающаяся гемиплегия детского возраста (AHC); мозжечковая атаксия, арефлексия, «полая» стопа, атрофия зрительного нерва и нейросенсорная тугоухость (CAPOS) [7].
Дистония-паркинсонизм с быстрым началом (RDP) наследуется по аутосомно-доминантному типу, дебютирует в возрасте от 4 до 58 лет, но в большинстве случаев встречается у детей. Симптомы могут быть вызваны широким спектром физических, эмоциональных или химических триггеров (например, спортивные нагрузки, роды, эмоциональный стресс, инфекционные заболевания, воздействие алкоголя). Клинические признаки классической RDP включают внезапное появление бульбарных симптомов и дистонии конечностей с признаками паркинсонизма (брадикинезия и постуральная нестабильность). Клиническая картина характеризуется рострокаудальной направленностью развития патологических изменений (лицо > рука > нога) с их явным прогрессированием в течение короткого промежутка времени (от нескольких минут до 30 дней), стабилизацией в течение 1 мес. и последующими минимальными изменениями на протяжении жизни, в т. ч. незначительной регрессией. Под воздействием леводопы или дофаминергических агонистов симптомы дистонии обычно не купируются. Помимо признаков органического поражения центральной нервной системы у некоторых пациентов с классической RDP могут наблюдаться такие симптомы, как депрессия, тревога, социальные фобии [4].
В редких случаях заболевание может дебютировать со слабовыраженной дистонии конечностей в сочетании с тремором, также возможно развитие судорожного компонента спустя годы после начала заболевания. При атипичных формах возможен дебют в виде симптомов мозжечковой атаксии и гиперкинезов [6]. В литературе также описаны случаи «повторного начала» или резкого ухудшения состояния в позднем возрасте.
В своей статье мы приводим собственный клинический опыт наблюдения и постановки диагноза у ребенка с одним из вариантов течения дистонии-плюс, а именно с дистонией-паркинсонизмом с быстрым началом (RDP, DYT12).
Клиническое наблюдение
Больной С., 12 лет, в июне 2018 г. поступил в стационар с жалобами на лихорадку до 38,5 °C, расстройство речи, выраженные псевдобульбарные расстройства в виде нарушения глотания, слюнотечения, дисфонии, дисфагии, а также на эпизоды насильственного смеха, общую слабость. Из анамнеза известно о его пребывании до госпитализации в Азиатском регионе с 30.05.2018. по 20.06.2018. Заболел остро 03.06.2018: температура поднялась до субфебрильных цифр, появились боль и першение в горле, общая слабость, самостоятельно принимал жаропонижающие и противовирусные препараты без видимого эффекта. С 08.06.2018 появилась выраженная головная боль и многократная неукротимая рвота, не приносящая облегчения. Обратились в госпиталь по месту пребывания, где было проведено обследование и назначено симптоматическое лечение (выписки не были предоставлены). На фоне лечения в стационаре улучшения состояния не наблюдалось, через 10 дней присоединились псевдобульбарные нарушения в виде дизартрии и слюнотечения, а также эпизоды насильственного смеха и необоснованного возбуждения. Сразу по прибытии в г. Красноярск бригадой скорой помощи доставлен в инфекционное отделение КГБУЗ «КМДКБ № 1» с подозрением на менингоэнцефалит.
За период госпитализации с июня по июль 2018 г. были проведены лабораторные исследования, получены положительные результаты иммуноферментного анализа крови на лихорадку Западного Нила и вирусологического исследования ликвора на РНК энтеровирусов. При проведении магнитно-резонансной томографии головного мозга и шейно-грудного отдела спинного мозга с внутривенным контрастированием была выявлена картина спинального лептоменингита на уровне С3-Тh1 и кистозно-глиозные изменения поствоспалительного генеза в передних отделах правого полушария и червя мозжечка справа. На электронейромиографии (ЭНМГ) (стимуляционной и игольчатой) было выявлено умеренно выраженное снижение амплитуды М-ответа по моторным волокнам лицевого нерва с обеих сторон.
На фоне лечения симптомы частично купированы, сохранились периодические тикоидные подергивания мимической мускулатуры, дизартрия, тремор языка и кистей обеих рук, патологическая установка рук при напряжении. При выписке был выставлен диагноз «Энцефаломиелополирадикулоневрит, тяжелый, вялый периферический тетрапарез, парез лицевого нерва с двух сторон, псевдобульбарный синдром, острое течение».
Через 1 мес. после выписки из инфекционного отделения, в сентябре — октябре 2018 г. проходил реабилитационное лечение в неврологическом отделении КГБУЗ «КМДКБ № 1» г. Красноярска. На момент госпитализации предъявлял жалобы на слабость в руках, затруднение тонкой моторики рук, слабость в ногах при ходьбе, дизартрию, насильственные подергивания рук, пальцев кистей и плеч, усиливающиеся при волнении или напряжении. В неврологическом статусе обращали на себя внимание такие симптомы, как брадипсихия, брадикинезия, ригидность мышечного тонуса по типу «зубчатого колеса». За время нахождения в отделении были исключены генетически детерминированные лизосомные и митохондриальные заболевания. По заключению ЭНМГ (стимуляционной и игольчатой) наблюдалось снижение М-сигнала по сенсорным волокнам икроножного нерва справа и малоберцового слева. Получил курс иммуноглобулина человека внутривенно в дозе 2 г/кг массы тела № 5 с дальнейшим введением в такой же дозе 1 р./мес. в течение 6 мес., холина альфосцерат по 400 мг 2 р./сут в течение 1 мес., на фоне лечения отмечалась незначительная положительная динамика.
Третья госпитализация была в марте — апреле 2019 г. по поводу отсутствия положительной динамики на фоне приема иммуноглобулинов. Отмечалось усугубление проявлений симптомов поражения экстрапирамидной системы в виде усиления постурально-кинетического тремора не только рук, но и головы, насильственное открывание рта, проявления оромандибулярной дискинезии, более выраженная постуральная неустойчивость при ходьбе. В течение прошедших 4 мес. сформировалась контрактура правого голеностопного сустава. Во время нахождения в отделении в качестве поддерживающей терапии были назначены леводопа 100 мг + бенсеразид 25 мг в 2 приема, на фоне терапии наблюдалась минимальная положительная динамика.
С учетом течения заболевания было заподозрено наследственное прогрессирующее дегенеративное заболевание нервной системы, выставлен предположительный диагноз «DYT1» и назначено молекулярно-генетическое обследование. По результатам применения таргетной панели на нейродегенеративные заболевания выявлена мутация в гене АТР1А3 и сформулирован окончательный диагноз: «Миогенная дистония: тип DYT12, с аутосомно-доминантным типом наследования, дистония-паркинсонизм с быстрым началом (RDP)».
На момент написания статьи пациент получает лечение препаратом клоназепам в дозе 2 мг/сут с минимальной положительной динамикой, находится на домашнем обучении в общеобразовательной школе.
Заключение
Таким образом, данный клинический случай демонстрирует сложность диагностического поиска при наследственных дистониях, что может быть обусловлено множеством факторов, таких как наличие симптомов, схожих с проявлениями других заболеваний с клинической картиной поражения нервной системы, в т. ч. инфекционных патологий. Это является одной из причин недостаточной выявляемости данной патологии наряду с ее малой встречаемостью в популяции. Также группа заболеваний с признаками дистонии характеризуется выраженным фенотипическим полиморфизмом, что значительно расширяет диагностические границы и влияет на сроки постановки диагноза.
Только для зарегистрированных пользователей
Мышечные дистонии
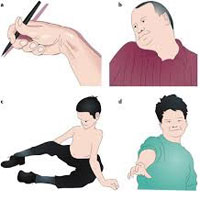
Симптомы дистонии
Мышечная дистония может быть в различных частях тела. Ранние симптомы могут включать в себя ухудшение почерка после написания нескольких строк, судороги в ногах или скованность в мышцах ног, могут возникать неожиданно как «гром среди ясного неба» или возникать после бега или ходьбы на некоторое расстояние. Возможно непроизвольное скручивание шеи, особенно после нагрузки или стресса. Иногда возникает непроизвольное частое моргание глаз, что может приводить к функциональной слепоте. Другие возможные симптомы это тремор и нарушения речи. Начальные симптомы могут быть очень незначительными и могут быть заметны только после длительных нагрузок, стресса или усталости. Со временем симптомы могут стать более явными и стойкими, но, иногда, они могут не прогрессировать.
У некоторых пациентов, симптомы дистонии появляются в детстве, в возрастном промежутке от 5 до 16 лет, чаще всего, в конечностях (ноге или в руке). При генерализованной дистонии дистонические движения могут быстро прогрессировать и вовлекать все конечности и туловище, но скорость прогрессирования обычно заметно замедляется после завершения пубертатного возраста.
У других пациентов, симптомы появляются в конце подросткового или раннего взрослого возраста. В таких случаях, дистония нередко начинается в верхних частях тела, а симптоматика прогрессирует медленно. Дистония, которая начинается в зрелом возрасте, чаще всего, остается фокальной или сегментарной дистонией.
Прогрессирование дистонии проходит несколько стадий. Первоначально дистонические движения преходящие и появляются только во время произвольных движений или стресса. В дальнейшем, у пациентов могут возникать дистонические ненормальные позы и движения во время ходьбы и, в конечном счете, даже в состоянии покоя. Дистонические движения могут со временем привести к стойким физическим дефектам, так как возникают укорочения сухожилий.
При вторичных дистониях вследствие травмы или инсульта у пациентов отмечаются аномальные движения только с одной стороны тела, которые могут появиться сразу после травмы головного мозга (инсульта) или через некоторое время после. Симптомы обычно не прогрессируют и не охватывают другие части тела.
Классификация дистоний
Одна из классификаций дистонии подразделяет их в зависимости от частей тела, вовлеченных в это состояние:
Некоторые типы дистонии выделяются как отдельные синдромы:
Торсионная дистония, которая ранее называлась мышечная деформирующая дистония является редкой формой дистонии, имеет генетическую детерминированность, обычно начинается в детстве и неуклонно прогрессирует. Торсионная дистония приводит к выраженным физическим дефектам и нередко к тяжелой инвалидизации. Исследования генетиков выявили причину этой формы дистонии (у многих пациентов имелись мутации в гене под названием DYT1). Было также отмечено, что этот ген ассоциирован не только с генерализованной дистонией, но и с некоторыми формами фокальной дистонии. Тем не менее, есть данные, что большинство дистоний не связаны с этим дефектом гена и имеют неизвестную причину.
Краниальная дистония это термин, используемый для описания дистонии, которая влияет на мышцы головы, лица и шеи. Оромандибулярная дистония затрагивает мышцы челюсти, губ и языка. Челюсть, может выдвигаться вперед, опускаться или закрываться и возможны нарушения глотания и речи. Спастические дисфония поражает мышцы гортани, которые контролируют речь, что может вызвать нарушения речи, дыхания или хриплость голоса. Синдром Мейга является сочетанием блефароспазма и оромандибулярной дистонии и иногда спастической дисфонии.Спастическая кривошея также иногда классифицируется, как краниальная дистония.
Как правило, ДЗД начинается в детстве или в подростковом возрасте, с прогрессирующим ухудшением процесса ходьбы, а в некоторых случаях и наличием спастичности. При дистонии Segawa, симптомы могут колебаться в течение дня от относительной мобильности утром, с постепенным ухудшением в дневное и вечернее время, а также после физических упражнений. Диагноз ДЗД может быть не выставлен своевременно, так как эта форма дистонии по проявлениям напоминает по симптоматике церебральный паралич. Кроме того, существуют формы дистонии, которые могут иметь четкую генетическую причину: DYT1 дистония является редкой формой доминантно наследуемой генарализованной дистонии, которая может быть вызваны мутацией в гене DYT1. Эта форма дистонии обычно начинается в детстве, сначала влияет на конечности, и неуклонно прогрессирует, часто вызывая инвалидизацию. Поскольку эффекты мутации гена проявляются не всегда, у некоторых людей с наличием мутации этого гена может не быть проявлений дистонии.
В последнее время исследователи выявили еще одну генетическую причину дистонии связанную связано с мутациями в гене DYT6. Дистония вызванная мутацией в гене DYT6 часто проявляется как черепно-лицевая дистония, цервикальная дистонии или дистония руки.
Механизм развития дистонии
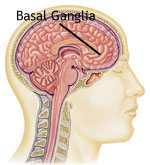 Ученые считают, что дистонии возникают в результате нарушений функционирования в области мозга, которая называется базальные ганглии, где происходит обработка информации от импульсов, которые поступают в мозг при сокращениях мышц. Ученые предполагают, что происходит нарушение выработки организмом определенной группы химических веществ (нейротрансмиттеров), которые позволяют клеткам мозга взаимодействовать друг с другом. Некоторые из этих нейротрансмиттеров включают:
Ученые считают, что дистонии возникают в результате нарушений функционирования в области мозга, которая называется базальные ганглии, где происходит обработка информации от импульсов, которые поступают в мозг при сокращениях мышц. Ученые предполагают, что происходит нарушение выработки организмом определенной группы химических веществ (нейротрансмиттеров), которые позволяют клеткам мозга взаимодействовать друг с другом. Некоторые из этих нейротрансмиттеров включают:
Приобретенные дистонии, которые также называются вторичные дистонии, являются результатом влияния экзогенных факторов или заболеваний, приводящих к повреждению базальных ганглиев. Родовая травма (в частности, из-за гипоксии мозга), некоторые инфекции, реакция на некоторые лекарства, тяжелые металлы или отравления окисью углерода, травмы, или инсульт могут привести к появлению дистонических симптомов. Дистонии также могут быть симптомами других заболеваний, некоторые из которых могут быть наследственными.
Около 50% случаев дистонии не имеют никакой связи с заболеваниями или травмами и называются первичной или идиопатической дистонией.
Некоторые случаи первичной дистонии могут иметь различные типы наследственных паттернов.
Лечение
 В настоящее время не существует медикаментов, которые могут предотвратить развитие дистонии или замедлить прогрессирование. Однако существует несколько вариантов лечения, которые могут облегчить некоторые симптомы дистонии, поэтому врачи могут подобрать каждому пациенту определенную тактику лечения, основанную на конкретных симптомах.
В настоящее время не существует медикаментов, которые могут предотвратить развитие дистонии или замедлить прогрессирование. Однако существует несколько вариантов лечения, которые могут облегчить некоторые симптомы дистонии, поэтому врачи могут подобрать каждому пациенту определенную тактику лечения, основанную на конкретных симптомах.
Хирургические методы лечения в некоторых случаях могут быть рекомендованы отдельным пациентам, когда лекарства оказываются не эффективны или побочные эффекты являются слишком серьезными. В отдельных случаях при выраженной генерализованной дистонии проводится хирургическая деструкция части таламуса, глубокой структуры мозга контролирующей движения. Нарушение речи является основным риском такой процедуры, так как таламус располагается около структур головного мозга, контролирующих речь. Хирургическая денервация мышц иногда помогает при фокальной дистонии, в том числе при блефароспазме, спазматической дисфонии и кривошее. Но результаты таких денерваций не очень обнадеживающие в долгосрочной перспективе.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Диагностика и лечение экстрапирамидных гиперкинезов
Экстрапирамидные гиперкинезы относятся к числу расстройств, которые не столько угрожают жизни, сколько «разрушают» ее, значительно ограничивая функциональные возможности пациентов, приводя их к психологической и социальной изоляции. Длительное время ре
Экстрапирамидные гиперкинезы относятся к числу расстройств, которые не столько угрожают жизни, сколько «разрушают» ее, значительно ограничивая функциональные возможности пациентов, приводя их к психологической и социальной изоляции. Длительное время результаты лечения экстрапирамидных гиперкинезов вызывали лишь разочарование как у самих пациентов, так и у врачей. Но в последние десятилетия ситуация начала меняться. Появились более четкие критерии диагностики различных вариантов экстрапирамидных гиперкинезов, существенно расширились возможности лечения, как за счет появления новых методов, так и за счет более рационального применения ранее существовавших. И если мы до сих пор в подавляющем большинстве случаев не можем кардинально излечить гиперкинез, то, по крайней мере, способны существенно улучшить качество жизни многих пациентов. В данной статье рассмотрены современные подходы к диагностике и лечению наиболее частых вариантов экстрапирамидных гиперкинезов.
Определение и классификация экстрапирамидных гиперкинезов
Экстрапирамидные гиперкинезы (или дискинезии) — это непроизвольные (насильственные) избыточные движения, обусловленные поражением базальных ганглиев и связанных с ними структур, условно объединяемых в экстрапирамидную систему [9]. Экстрапирамидные гиперкинезы следует отличать от более редких периферических гиперкинезов, связанных с поражением или дисфункцией периферических нервов (например, лицевого гемиспазма, синдрома «болезненных ног (рук) — движущихся пальцев», тетания и др.), а также от психогенных гиперкинезов, являющихся соматическим выражением того или иного психического заболевания.
К основным экстрапирамидным гиперкинезам относят тремор, дистонию, хорею, атетоз, баллизм, тики, миоклонию, акатизию [11]. Традиционно считается, что каждый гиперкинез имеет свой неповторимый двигательный рисунок, в основе которого лежит уникальный патофизиологический механизм. Отчасти это действительно так. Тем не менее накопленный нами опыт позволяет говорить не столько об отдельных, дискретных синдромах, сколько о едином спектре (континууме) синдромов, в котором наряду с изолированными формами широко представлены переходные или комбинированные формы, что существенно затрудняет их синдромальную диагностику и выбор правильного лечения.
Справедливо мнение, что гиперкинезы «сопротивляются» жесткой вербальной категоризации, и их значительно проще узнать, чем описать. Ситуация усложняется еще и тем обстоятельством, что один и тот же гиперкинез в разных частях тела может выглядеть по-разному. В связи с этим распознавание гиперкинезов, особенно в сложных или переходных случаях, невозможно без выделения ограниченного числа ключевых признаков. По нашему мнению, особенно важное значение имеют три признака: двигательный рисунок, временной рисунок, характер возникновения.
По двигательному рисунку гиперкинезы могут быть разделены на три основные группы:
По временному рисунку гиперкинезы могут быть разделены на две группы:
По характеру возникновения непроизвольные гиперкинезы могут быть разделены на четыре основные группы:
Феноменологические особенности основных форм экстрапирамидных гиперкинезов, в сравнении с психогенными гиперкинезами, представлены в таблице.
Общие принципы диагностики экстрапирамидных гиперкинезов
Распознавание того или иного экстрапирамидного синдрома — только отправная точка сложной диагностической работы, итогом которой может быть установление нозологического диагноза.
Диагностика экстрапирамидного синдрома включает три последовательных этапа.
С нозологической точки зрения в рамках любого экстрапирамидного гиперкинеза могут быть выделены три основные формы.
Большинство случаев экстрапирамидных гиперкинезов имеют первичный (идиопатический) характер, однако их диагностика требует исключения других, прежде всего вторичных, форм гиперкинезов, особенно связанных с курабельными заболеваниями (такими, как опухоли или эндокринопатии), а также курабельных форм мультисистемных дегенераций, в первую очередь гепатолентикулярной дегенерации (болезни Вильсона–Коновалова). Подобные случаи в клинической практике встречаются редко, но именно они должны быть исключены в первую очередь. Исключение вторичной природы гиперкинеза может потребовать дополнительного инструментального (КТ или МРТ головного мозга, ЭЭГ) либо лабораторного исследования. Следует помнить, что любой экстрапирамидный синдром, впервые проявившийся в возрасте до 50 лет, служит основанием для исключения гепатолентикулярной дегенерации (для этого требуется как минимум анализ крови на церулоплазмин и исследование роговицы с помощью щелевой лампы с целью обнаружения пигментного кольца Кайзера–Флейшера) [12].
Наконец, в каждом случае гиперкинеза следует подумать и о том, что он может иметь психогенную природу. В прошлом большинство случаев гиперкинезов нередко рассматривались как психогенные расстройства. Этому способствовали вариабельность и динамичность проявлений экстрапирамидных гиперкинезов, их зависимость от движений, позы, эмоционального состояния пациента, нередкое присутствие у пациентов с первичными формами гиперкинезов аффективных расстройств. В настоящее время очевидно, что психогенные гиперкинезы встречаются редко, но тем более важным представляется их своевременное выявление, позволяющее проводить целенаправленное лечение и как минимум избавляющее пациента от ненужной,
а иногда и опасной для него терапии.
В пользу психогенной природы гиперкинеза могут свидетельствовать: острое начало, последующее волнообразное течение с периодами длительных спонтанных ремиссий, непостоянство гиперкинеза, причудливость его рисунка, обычно не соответствующего характерным формам экстрапирамидных гиперкинезов, ослабление при отвлечении внимания, стойкая реакция на плацебо, полная резистентность к стандартной терапии, наличие других псевдоневрологических симптомов с феноменом селективной несостоятельности, выраженных аффективных расстройств, сопровождающихся множественными соматоформными жалобами, наличие рентной ситуации (в которой больной извлекает моральную или, реже, материальную выгоду из своего заболевания) и т. д. [1].
Ниже более подробно рассмотрены подходы к диагностике и лечению четырех наиболее часто встречающихся форм экстрапирамидных гиперкинезов: тремора, дистонии, хореи и тиков.
Тремор
Тремор (дрожание) — самый частый экстрапирамидный гиперкинез, характеризующийся непроизвольными ритмичными колебательными движениями части тела (чаще всего конечностей и головы) или всего тела, которые упорядочены во времени и пространстве. Феноменологически выделяют два основных типа тремора: тремор покоя и тремор действия (акционный тремор). Тремор покоя характерен для синдрома паркинсонизма, и прежде всего болезни Паркинсона.
Тремор действия подразделяют на постуральный, возникающий при удержании определенной позы (например, вытянутых рук), кинетический, появляющийся при движении (в том числе при приближении к цели — так называемый интенционный тремор), изометрический — при изометрическом мышечном сокращении (например, при сжимании кисти в кулак). К особым формам тремора относятся ортостатический тремор, развивающийся при переходе в вертикальное положение и стоянии, а также селективный кинетический тремор (возникающий только при определенных движениях, например при письме — писчий тремор).
Основной формой первичного тремора является эссенциальный тремор (ЭТ), представляющий собой самостоятельное заболевание, преимущественно проявляющееся постурально-кинетическим тремором рук, реже головы, голосовых связок, ног, туловища. Более чем в половине случаев заболевание носит семейный характер. Анализ семейных случаев указывает на аутосомно-доминантный тип наследования, однако установить генетический дефект удалось лишь в отдельных случаях [4]. Не исключено, что спорадические случаи, как правило, проявляющиеся в более позднем возрасте (часто после 60 лет), носят мультифакторный характер и связаны как с генетическим дефектом, так и с воздействием неидентифицированных внешних факторов. ЭТ начинается постепенно, обычно с постурального дрожания в руках, которое может быть как симметричным, так и асимметричным. Со временем амплитуда и распространенность тремора нарастают, тогда как его частота снижается (от 6–8 до 4 Гц). Резко выраженный постуральный тремор может сохраняться и в покое. Помимо косметического дефекта, тремор может нарушать функцию верхних конечностей: больным становится все труднее принимать пищу, писать, играть на музыкальных инструментах, выполнять другие тонкие действия. Однако в некоторых случаях, несмотря на существование заболевания в течение нескольких десятилетий, инвалидизации не наступает.
Другие неврологические проявления обычно отсутствуют, но примерно у трети больных выявляются минимальные проявления мозжечковой атаксии (например, нарушения тандемной ходьбы), минимальная гипомимия, иногда миоклония и фокальная дистония. У больных ЭТ чаще, чем в среднем в популяции, наблюдаются артериальная гипертензия, нейросенсорная тугоухость, когнитивные нарушения.
Как особые варианты ЭТ рассматривают первичный ортостатический тремор, изолированный тремор головы, а также тремор, возникающий при письме (писчий тремор). Последний занимает промежуточное положение между тремором и дистонией. Изолированный тремор головы, возникающий на фоне ее дистонической позы, как правило, представляет собой дистонический тремор, являясь вариантом фокальной дистонии (см. ниже).
ЭТ необходимо также дифференцировать с усиленным физиологическим тремором, возникающим при волнении, утомлении, под действием холода и некоторых лекарственных средств, при абстинентном синдроме, тиреотоксикозе, гипогликемии, интоксикациях; мозжечковым (преимущественно интенционным) тремором, тремором Холмса (асимметричным крупноразмашистым дрожанием, которое представляет собой комбинацию постурального и кинетического тремора с тремором покоя и возникает при очаговых поражениях среднего мозга или таламуса), тремором при полиневропатиях [3].
До сих пор в клинической практике возникают большие сложности при дифференциальной диагностике ЭТ с болезнью Паркинсона. Для последней, в отличие от ЭТ, характерны присутствие других симптомов паркинсонизма, прежде всего выраженной гипокинезии, более быстрое прогрессирование, выраженная асимметрия проявлений, преобладание тремора покоя, отсутствие тремора головы, иная последовательность вовлечения конечностей (рука–ипсилатеральная нога–контралатеральные конечности; при ЭТ: рука–контралатеральная рука–ноги), лечебный эффект противопаркинсонических средств.
К сожалению, в настоящее время возможности предупредить или хотя бы замедлить прогрессирование заболевания не существует. Тем не менее значительная часть пациентов с ЭТ не нуждается ни в каком ином лечении, кроме как в рациональной психотерапии, заключающейся в разъяснении доброкачественной природы заболевания. Если тремор существенно нарушает функцию рук, его можно частично уменьшить почти у 2/3 больных с помощью средств первого ряда — β-блокаторов (пропранолол, 60–360 мг/сут) и примидона (гексамидин, 125–500 мг/сут). Выбор препарата производят исходя из риска побочного действия, сопутствующих заболеваний и индивидуальных особенностей пациентов. У молодых больных, а также пациентов с артериальной гипертензией чаще применяют β-блокаторы, тогда как у пожилых пациентов, особенно чувствительных к побочному действию пропранолола на сердечно-сосудистую систему, более целесообразен прием примидона, который к тому же в большинстве случаев достаточно применять всего 1 раз в сутки — перед сном [5]. Чтобы улучшить переносимость примидона, его терапевтическая доза подбирается путем медленного титрования. После достижения эффективной дозы побочные эффекты наблюдаются редко. В резистентных случаях возможна комбинация двух препаратов первого ряда либо их назначение в сочетании с препаратами второго ряда, к которым относятся клоназепам и алпразолам (особенно эффективны при кинетическом треморе и треморе головы), фенобарбитал, антагонисты кальция (флунаризин, нимодипин), габапентин, топирамат и теофиллин. При треморе головы и голосовых связок единственный метод, дающий гарантированный эффект, — регулярные инъекции ботулотоксина. В наиболее резистентных случаях прибегают к клозапину или проводят стереотаксическое нейрохирургическое вмешательство на таламусе.
Коррекция усиленного физиологического тремора включает прекращение действия провоцирующего фактора, применение β-блокаторов (например, пропранолола). При мозжечковом треморе, обычно плохо поддающемся лечению, обычно назначают ГАМКергические препараты (клоназепам, вальпроевую кислоту, баклофен, габапентин), карбамазепин, пропранолол, примидон, амантадин, практикуется также утяжеление конечности с помощью браслета. В наиболее тяжелых случаях возможно применение изониазида. При треморе Холмса иногда эффективны холинолитики, препараты леводопы, агонисты дофаминовых рецепторов, клоназепам, клозапин, комбинация вальпроевой кислоты и пропранолола, введение ботулотоксина.
Дистония
Дистония — синдром, характеризующийся медленными (тоническими) или повторяющимися быстрыми (клонико-тоническими) движениями, вызывающими вращение (отсюда термин «торсионная дистония» — от лат. torsio — вращение, скручивание), сгибание или разгибание туловища и конечностей с формированием патологических поз.
В отличие от более быстрого и хаотичного хореического гиперкинеза (см. ниже) рисунок дистонического гиперкинеза более стереотипен и упорядочен [1, 2]. Дистонические феномены многообразны и включают преходящие дистонические спазмы, которые иногда бывают столь быстрыми, что напоминают миоклонию (при «клонической» форме дистонии) или относительно ритмичный дистонический тремор, обычно усиливающийся при попытке больного преодолеть дистоническую позу.
Характерная особенность дистонического гиперкинеза — возникновение или усиление при произвольных движениях. Дистоническая поза первоначально имеет преходящий характер, возникает лишь при определенном движении, но постепенно становится постоянной, сохраняясь и в покое. Эта эволюция дистонии весьма характерна, наряду с другими проявлениями динамичности гиперкинезов: улучшение после сна, влияние корригирующих жестов и изменений позы (дистония часто усиливается в вертикальном положении и уменьшается в горизонтальном), наличие парадоксальной кинезии (уменьшение гиперкинеза при изменении привычного двигательного стереотипа), колебания симптоматики, влияние эмоционального состояния. Признаки динамичности гиперкинезов, включая возможность кратковременной произвольной коррекции патологической позы, позволяют отличить дистонию от заболеваний скелетно-мышечной системы, вызывающих более фиксированные изменения позы (псевдодистонии).
По распространенности гиперкинеза выделяют:
Почти 90% случаев составляет первичная (идиопатическая) дистония, которая проявляется только дистоническим гиперкинезом и имеет наследственный характер, но бывает представлена как семейными, так и спорадическими случаями. При раннем дебюте (до 15 лет) дистония обычно имеет четко наследственный характер, часто начинается с одной ноги, а затем генерализуется, вовлекая туловище. При более позднем начале (после 21 года) дистония чаще оказывается представлена спорадическими случаями, первично вовлекает мышцы верхней части тела, а в дальнейшем чаще остается фокальной. В классическом варианте она наследуется по аутосомно-доминантному типу и связана с мутацией в локусе DYT1 на 9-й хромосоме, кодирующем белок торсин А. Реже встречаются другие варианты генерализованной дистонии с наследованием по аутосомно-рецессивному или рецессивному, сцепленному с Х-хромосомой типу [4].
Фокальные формы встречаются примерно в 10 раз чаще, чем генерализованные. К числу частых фокальных вариантов относятся краниальная дистония, включающая блефароспазм и оромандибулярную (орофациальную) дистонию, и цервикальная дистония. Сочетание орофациальной дистонии с гиперкинезом других мышц лица, в том числе с блефароспазмом и дистонией мышц шеи (сегментарная краниоцервикальная дистония), обозначают как синдром Мейжа.
В некоторых семейных случаях сегментарной краниоцервикальной дистонии, при которой имеется сочетание спастической кривошеи с блефароспазмом и орофациальной дистонией, выявляется генетический дефект (ген DYT6 на 8-й хромосоме). В семейных случаях чисто цервикальной дистонии выявлен патологический ген DYT7 на 18-й хромосоме. Однако причина большинства случаев цервикальной дистонии остается неясной (идиопатическая цервикальная дистония) [4].
В последние годы выделена группа заболеваний, условно обозначаемых как дистония-плюс, при которых дистонический гиперкинез сопровождается другими экстрапирамидными расстройствами, в частности симптомами паркинсонизма (дистония/дистония-паркинсонизм, чувствительная к L-ДОФА, или ДОФА-зависимая, дистония, или болезнь Сегавы) или миоклонией (миоклоническая дистония).
Вторичная (симптоматическая) дистония составляет не более 5–10% случаев дистонии. Чаще всего она возникает после очагового повреждения базальных ганглиев или таламуса (например, при инсульте), развиваясь спустя несколько месяцев, иногда на фоне регресса гемипареза («отставленная» дистония). Дистония конечности изредка возникает на фоне тяжелой рефлекторной симпатической дистрофии, развившейся после периферической травмы. Важнейшей причиной вторичной дистонии служит воздействие лекарственных средств, прежде всего нейролептиков, метоклопрамида, препаратов леводопы.
Наиболее курабельны ДОФА-зависимые формы дистонии (например, болезнь Сегавы), при которых эффективны малые дозы препаратов леводопы (суточную дозу — от 0,25 до 1,5 табл. накома или мадопара 250 — назначают в один или два приема). Поскольку ДОФА-зависимую дистонию не всегда удается дифференцировать клинически, препараты леводопы целесообразно испробовать во всех случаях генерализованной дистонии, развившейся в детском и юношеском возрасте.
В целом при генерализованной дистонии можно рекомендовать назначение препаратов в следующей последовательности: препараты леводопы (в детском и юношеском возрасте); холинолитики (обычно в высокой дозе, например до 100 мг циклодола в сутки); баклофен; клоназепам и другие бензодиазепины; карбамазепин (финлепсин); препараты, истощающие запасы дофамина в пресинаптических депо (резерпин); нейролептики — блокаторы дофаминовых рецепторов (галоперидол, пимозид, сульпирид, фторфеназин); комбинация из перечисленных средств (например, холинолитика с резерпином и нейролептиком).
Следует отметить, что во многих случаях эффекта удается добиться лишь при применении высоких доз лекарственных средств. В резистентных случаях прибегают к стереотаксическим операциям на бледном шаре или таламусе.
Наиболее эффективный метод лечения фокальных дистоний — инъекции ботулотоксина (ботокса или диспорта) в мышцы, вовлеченные в гиперкинез. Ботулотоксин вызывает частичный парез этих мышц и тем самым устраняет дистонию на 3–6 мес, после чего инъекцию приходится повторять [7]. Возможности лекарственных средств весьма ограничены. При цервикальной дистонии эффекта иногда удается добиться с помощью клоназепама, баклофена или нейролептиков. При блефароспазме более эффективны клоназепам и холинолитики, при оромандибулярной дистонии — баклофен и холинолитики, при «писчем спазме» — холинолитики. В части случаев некоторого улучшения, которое носит скорее субъективный характер, можно добиться путем воздействия на мышцы, участвующие в гиперкинезе, с помощью различных физиотерапевтических процедур, а также применяя метод биологической обратной связи или специальную гимнастику. В резистентных случаях прибегают к периферической денервации мышц.
Хорея
Хорея характеризуется непрерывным потоком быстрых хаотичных, нерегулярных во времени и по амплитуде мультифокальных движений. Гиперкинез чаще всего вовлекает дистальные отделы конечностей, мимические мышцы, иногда мышцы глотки, гортани, туловища. Насильственные движения напоминают гримасничанье, кривляние, нарочитые ужимки, танцевальные движения (греч. choreia — пляска) [8].
К наиболее частым формам хореи относится болезнь Гентингтона (БГ) — наследственное заболевание, передающееся по аутосомно-доминантному типу, связанное с прогрессирующей дегенерацией нейронов подкорковых ядер и коры и проявляющееся главным образом сочетанием хореи с деменцией [4]. Тем не менее хорея — не единственное, а в ряде случаев и не основное проявление заболевания, поэтому термин «болезнь Гентингтона» предпочтительнее, чем термин «хорея Гентингтона». Генетический дефект при БГ выявлен на 4-й хромосоме и заключается в увеличении количества повторов («экспансии») одного из тринуклеотидных фрагментов в зоне ДНК, кодирующей белок гентингтин. В конечном итоге это предопределяет особую уязвимость и преждевременную гибель определенных популяций нейронов полосатого тела, прежде всего хвостатого ядра.
БГ обычно проявляется на 4–5-м десятилетии жизни и в дальнейшем неуклонно прогрессирует. Хорея обычно начинается с дистальных отделов конечностей, затем постепенно генерализуется и нарушает произвольные движения. Больные не могут долго держать высунутым язык или сжимать кисть в кулак, походка становится неустойчивой, «танцующей», иногда замедленной, напряженной. Со временем непроизвольные движения все более приобретают дистонический характер, присоединяются гипокинезия и ригидность, оживление рефлексов, грубая постуральная неустойчивость, приводящая к частым падениям. Уже на ранней стадии часто наблюдается выраженная дизартрия с замедленной аритмичной речью; дисфагия появляется на более поздней стадии и бывает причиной аспирации, ведущей к асфиксии или пневмонии. Психические расстройства многообразны и бывают представлены нарастающим когнитивным дефицитом, депрессией с нередкими суицидальными попытками, навязчивыми и фобическими расстройствами, психотическими нарушениями [9].
Малая хорея, являющаяся осложнением ревматизма и в прошлом составляющая значительную часть случаев вторичной хореи, в последние годы возникает исключительно редко. В связи с этим при возникновении хореи в детском или юношеском возрасте важно исключать иные причины синдрома: сосудистую хорею, системную красную волчанку, антифосфолипидный синдром и др. У пожилых людей хорея чаще бывает вызвана полицитемией, заболеваниями печени, последствиями инсульта.
При умеренном гиперкинезе с нейролептиками могут конкурировать средства, блокирующие глутаматергические рецепторы (например, амантадин или мемантин), некоторые антиконвульсанты (например, топирамат), а также симпатолитики (например, резерпин), истощающие запасы катехоламинов (в том числе дофамина) в депо пресинаптических терминалей. В некоторых случаях возможна комбинация лечебных средств, в частности нейролептика с антиглутаматергическими средствами, антиконвульсантами и симпатолитиками. Согласно некоторым данным длительный прием коэнзима Q10 и мемантина может несколько замедлять прогрессирование БГ. Важно с помощью нейролептиков и антидепрессантов корригировать сопутствующие психические расстройства, прежде всего депрессию, вспышки агрессии и неконтролируемого поведения [11].
При малой хорее средством выбора являются препараты вальпроевой кислоты и карбамазепины; только в том случае, если с их помощью не удается контролировать гиперкинез, назначают нейролептики в минимальной эффективной дозе. Кроме того, во избежание повторяющихся приступов ревматической лихорадки и развития порока сердца показана длительная пенициллинотерапия [9].
Тики представляют собой повторяющиеся отрывистые неритмичные движения, которые одномоментно вовлекают отдельные мышцы, группу мышц или часть тела. Тики возникают спонтанно на фоне нормальной двигательной активности и напоминают фрагменты целенаправленных движений. В отличие от многих других гиперкинезов больной может волевым усилием на определенное время (30–60 с) подавить тики, но обычно ценой быстро возрастающего внутреннего напряжения, которое неизбежно прорывается, вызывая кратковременную «бурю» тиков. Тикам может предшествовать ощущение непреодолимой потребности совершить движение, создающее иллюзию произвольности тика. Как правило, тики стереотипны и возникают в строго определенных у данного больного частях тела. Каждый больной имеет свой индивидуальный «репертуар» тиков, который меняется во времени. В отличие от других экстрапирамидных гиперкинезов тики сохраняются во сне [6].
Выделяют моторные, вокальные (фонические) и сенсорные тики, каждый из них, в свою очередь, делится на простые и сложные. К простым моторным тикам относят моргание, зажмуривание, подергивание головой, пожимание плечами, втягивание живота и др., к сложным — подпрыгивание, биение себя в грудь, эхопраксию (повторение жестов), копропраксию (воспроизведение неприличных жестов) и др. Простые моторные тики могут быть быстрыми, внезапными (клоническими) или более медленными и стойкими (дистоническими); например, к клоническим тикам относят моргание, а к дистоническим — зажмуривание (блефароспазм), окулогирные кризы, дистонические подергивания в области шеи, плеча, брюшных мышц. Простые вокальные тики включают покашливание, фырканье, похрюкивание, свист, сложные вокальные: эхолалию (повторение чужих слов); копролалию (произнесение непристойных слов); палилалию (повторение произнесенных самим больным слов или звуков). Сенсорные тики представляют собой кратковременные весьма неприятные ощущения, вынуждающие больного совершить движение. Они могут возникать в определенной части тела (например, в плече, кисти, животе или горле) и вынуждать больного совершать движение именно в этом регионе. По распространенности тики могут быть локальными (чаще в области лица, шеи, плечевого пояса), множественными или генерализованными.
Чаще всего тики имеют первичный характер, т. е. не связаны с каким-либо иным заболеванием, не сопровождаются другими двигательными синдромами, начинаются в детском и подростковом возрасте и обусловлены нарушением созревания связей между базальными ганглиями, лимбической системой и лобной корой. Мальчики страдают в 2–4 раза чаще, чем девочки [9].
Первичные тики условно подразделяют:
Есть основания полагать, что хронические моторные и вокальные тики и СТ, а возможно, и транзиторные тики могут быть проявлением одного и того же генетического дефекта, наследованного по аутосомно-доминантному типу. В то же время различия в выраженности гиперкинеза даже у однояйцевых близнецов указывают на важную роль внешних факторов, в частности действующих в перинатальном периоде [6].
Для СТ характерно волнообразное течение с периодами усиления и ослабления гиперкинеза, иногда с длительными спонтанными ремиссиями. Как правило, тики возникают у каждого больного в строго определенных частях тела. Каждый пациент имеет свой индивидуальный «репертуар» тиков, который меняется во времени. Обычно тики максимально выражены в подростковом периоде, а затем становятся слабее в юношеском и молодом возрасте. С наступлением зрелости примерно в трети случаев тики исчезают, у трети больных они значительно уменьшаются, а у оставшейся трети сохраняются в течение всей жизни, хотя и в этом случае редко приводят к инвалидизации. С возрастом уменьшается не только интенсивность тиков, но и их дезадаптирующее влияние. У большинства взрослых больных тики обычно не усиливаются, возможно лишь кратковременное ухудшение в период стрессовых ситуаций.
Более чем у половины больных с СТ выявляются сопутствующие психические расстройства (синдром навязчивых состояний, обсессивно-компульсивный синдром, синдром дефицита внимания с гиперактивностью), роль которых в социальной дезадаптации больного бывает подчас значительно выше, чем роль гиперкинеза.
Причиной вторичных тиков, которые встречаются реже, могут быть: повреждение головного мозга в перинатальном периоде, прием лекарственных препаратов (антиконвульсантов, нейролептиков, психостимуляторов и др.), черепно-мозговая травма, энцефалиты, сосудистые заболевания мозга, отравление угарным газом и т. д. При вторичных тиках гиперкинез обычно бывает менее динамичным (реже меняет локализацию, частоту, интенсивность), в меньшей степени оказываются выражены императивные позывы к движению и способность к подавлению гиперкинеза, могут присутствовать сопутствующие неврологические синдромы или такие психопатологические синдромы, как задержка психомоторного развития и умственная отсталость. Тиком иногда ошибочно называют доброкачественную миокимию век — преходящие подергивания круговой мышцы глаз, возникающие у вполне здоровых лиц при переутомлении, волнении, повышенном употреблении кофе или курении и не требующие лечения.
Во многих случаях при тиках медикаментозного лечения не требуется и достаточно успокоить больного и его родственников, рассказав о природе заболевания и указав на его доброкачественность. Важно отметить, что больному не угрожают снижение интеллекта, тяжелое психическое или неврологическое заболевание, и в подавляющем большинстве случаев такие пациенты хорошо социально адаптируются [9].
В легких случаях показано нефармакологическое воздействие в виде психопедагогической коррекции, обучения методам самоконтроля и саморегуляции. При умеренно выраженных тиках применяют бензодиазепины (клоназепам, 0,5–6 мг/сут) и другие ГАМКергические средства (баклофен, 20–75 мг/сут; фенибут, 250–1000 мг/сут). За рубежом для лечения умеренно выраженных тиков используют также клонидин и тетрабеназин. В более тяжелых случаях назначают «мягкие» нейролептики (сульпирид, 100–400 мг/сут; тиаприд, 200–400 мг/сут) либо атипичные нейролептики (например, рисперидон, 0,5–4 мг/сут или оланзапин, 2,5–5 мг/сут).
При резистентности к указанной терапии применяют большие дозы высокопотенциальных нейролептиков, комбинации двух нейролептиков с разным механизмом действия (например, рисперидона и тиаприда), комбинации нейролептика с антиконвульсантами (например, клоназепамом или топираматом) либо баклофеном. При тяжелых болезненных дистонических тиках, вовлекающих мышцы лица и шеи, возможно лечение ботулотоксином, который инъецируют в мышцы, участвующие в тике. Показан положительный эффект инъекций ботулотоксина в голосовые связки при вокальных тиках, в том числе при копролалии.
Для лечения сопутствующего синдрома нарушенного внимания и гиперактивности назначают ноотропные средства (пирацетам, пиридитол, глиатилин и др.), агонисты пресинаптических a2-адренорецепторов — клонидин и гуанфацин, малые дозы психостимуляторов, селегилин, трициклические антидепрессанты. Для лечения синдрома навязчивых состояний — антидепрессанты, ингибирующие обратный захват серотонина (кломипрамин, сертралин, флувоксамин и др.).
В лечении больных с тиками важное место принадлежит методам психотерапии. Они не способствуют уменьшению тиков, но, изменяя в благоприятную сторону отношение больных к тикам и корригируя сопутствующие психические нарушения, прежде всего синдром навязчивых состояний, улучшают социальную адаптацию больных. Обучение приемам релаксации позволяет больным снимать накапливающееся внутреннее напряжение. Разработаны специальные методики, тренирующие возможности больного произвольно контролировать тики (например, путем совершения конкурирующего движения при появлении ощущения, предваряющего тик).
Литература
О. С. Левин, доктор медицинских наук, профессор
