114. Дайте определения понятий.
Генетика – наука, изучающая закономерности наследственности и изменчивости живых организмов.
Наследственность – свойство всех живых организмов передавать свои признаки и свойства из поколения в поколение.
Изменчивость – свойство всех живых организмов приобретать в процессе индивидуального развития новые признаки.
115. Назовите ученого, которого по праву можно назвать основоположником генетики.
Грегор Мендель.
116. Дополните предложения.
Участок молекулы ДНК, или участок хромосомы, определяющий возможность развития определенного признака, называется ген.
В основе гибридологического метода лежит скрещивание организмов, отличающихся по каким-либо признакам, и в последующем анализ характера наследования этих признаков у потомства.
Если за проявления определенного признака отвечают два гена, расположенных в гомологичных хромосомах, то их называют аллели.
Организм, содержащий два одинаковых аллельных гена, называется гомозиготным.
Гетерозиготный организм содержит различные аллельные гены.
117. Дайте определения понятий.
Доминантный признак – признак, проявляющийся у гибридов.
Рецессивный признак – признак, подавляемый у гибридов.
119. Объясните, почему опыты, проведенные Г. Менделем с горохом, невозможно было провести с таким растением, как ястребинка (сем. Сложноцветные).
Растение ястребинка имеет цветки только жёлтого цвета и мелкие семена. Гибриды данного растения трудно поддаются генетическому анализу, тем более в 19 веке.
120. Проанализируйте представленную в учебнике схему наследования признаков при моногибридном скрещивании. Заполните пропуски в предложенном алгоритме решения задачи на моногибридное скрещивание.

121. Проанализируйте результаты, полученные в задании 120.
Ответьте на вопросы.
1) Сколько типов гамет образует растение с желтыми семенами?
2
2) Сколько типов гамет образует растение с зелеными семенами?
1
3) Какова вероятность появления растений с зелеными семенами?
50%
5) Сколько разных генотипов может быть среди гибридов первого поколения?
2
6) Сколько разных фенотипов может быть среди гибридов первого поколения?
2.
122. Решите задачу.
У человека ген длинных ресниц доминирует над геном коротких ресниц. Женщина с длинными ресницами, у отца которой были короткие ресницы, вышла замуж за мужчину с короткими ресницами. 1) Сколько типов гамет образуется у женщины? 2) Сколько типов гамет образуется у мужчины? 3) Какова вероятность в этой семье ребенка с длинными ресницами? 4) Сколько разных генотипов и сколько фенотипов может быть среди детей данной супружеской пары?
Решение:
А – длинные ресницы, а – короткие ресницы.
Так как у женщины отец был с короткими ресницами, то есть гомозиготным по рецессивному признаку, то у женщины с длинными ресницами генотип Аа (гетерозиготна). У ее мужа, как и у отца – аа.
Запишем схему скрещивания:

Расщепление по генотипу у детей будет Аа:аа, 1:1. По фенотипу длинные ресницы: короткие ресницы 1:1.
Ответ: у женщины образуется 2 типа гамет; у мужчины образуется 1 тип гамет; вероятность рождения детей с длинными ресницами 50%; среди детей данной супружеской пары может быть 2 разных генотипа (Аа, аа) и два разных фенотипа (длинные ресницы, короткие ресницы).
123. Решите задачу.
У собак висячее ухо доминирует над стоячим. От скрещивания гетерозиготных собак с висячим ухом с гомозиготными собаками, имеющими висячее ухо, получено 245 щенков. 1) Сколько типов гамет может образоваться у гомозиготной собаки? 2) Сколько различных генотипов и сколько фенотипов может быть в первом поколении?
Решение.
А –висячее ухо, а – стоячее ухо.
Скрещивали собак с генотипом Аа и АА.
Запишем схему скрещивания:

Все щенки будут с висячими ушами, расщепление по генотипу будет 1:1, ½ АА: ½ Аа.
Ответ: у гомозиготной собаки может образоваться 1 тип гамет. В первом поколении будет 2 различных генотипа и 1 фенотип.
Ген диабета рецессивен по отношению
Существуют два основных типа сахарного диабета: I тип (инсулинзависимый — ИЗСД) и II тип (инсулиннезависимый — ИНСД), составляющие 10 и 88% всех случаев соответственно. Они отличаются типичным возрастом начала, конкордантностью однояйцовых близнецов и ассоциацией с конкретными аллелями главного комплекса гистосовместимости (МНС — major histocompatibility complex). Семейное накопление наблюдают при обоих типах сахарного диабета, но в одной семье обычно присутствует только I или II тип.
Сахарный диабет I типа встречается в белой популяции с частотой около 1 на 500 (0,2%), в африканских и азиатских популяциях — реже. Обычно его обнаруживают в детстве или юности, и он вызван аутоиммунным поражением b-клеток поджелудочной железы, вырабатывающих инсулин. У преобладающего большинства больных детей уже в раннем детстве, задолго до развития явных проявлений болезни, вырабатываются многочисленные аутоантитела против ряда эндогенных белков, включая инсулин.
Ассоциация главного комплекса гистосовместимости при сахарном диабете I типа
При I типе сахарного диабета существует подтверждение роли генетических факторов: конкордантность однояйцовых близнецов приблизительно 40%, что далеко превышает 5% конкордантности у разнояйцовых. Риск диабета I типа для сибсов больного пробанда около 7%, что дает показатель наследуемости hs = 7% / 0,2% =- 35. Давно известно, что локус МНС — основной генетический фактор при сахарном диабете, так как около 95% всех пациентов с сахарным диабетом I типа (по сравнению с примерно 50% в нормальной популяции) — гетерозиготные носители аллелей HLA-DR3 или HLA-DR4 в локусе HLA класса II в МНС [HLA — человеческие лейкоцитарные антигены (human leucocyte antigens)].
Первое исследование, показавшее ассоциацию HLA-DR3 и HLA-DR4 с сахарным диабетом I типа при использовании стандартных методов проверки достоверности различия между разными аллелями HLA, проводили методом иммунологических реакций in vitro. Позже этот метод заменили прямым определением ДНК-последовательности разных аллелей. Секвенирование локуса гистосовместимости у огромного количества больных обнаружило, что «аллели» DR3 и DR4 — не просто аллели.
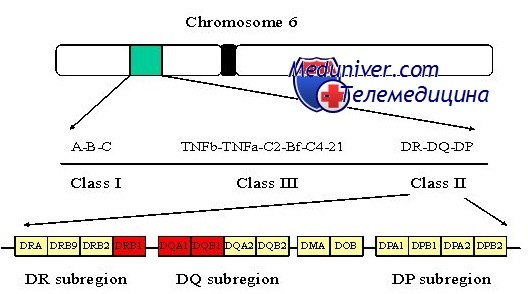
Как DR3, так и DR4 могут быть подразделены на десятки аллелей, располагающихся в локусе, теперь называющемся DRB1, и определяемых на уровне последовательности ДНК. Кроме того, стало ясным, что ассоциация между определенными аллелями DRB1 и сахарным диабетом I типа частично вызвана аллелем в другом локусе класса II, DQB1, располагающимся примерно в 80 килобазах от DRB1, вместе формирующих общий гаплотип (вследствие неравновесного сцепления; см. главу 10) друг с другом. DQB1 кодирует b-цепь, одну из цепей, формирующих димер белка класса II DQ. Оказывается, что присутствие аспарагиновой кислоты (Asp) в 57 позиции b-цепи DQ тесно связано с устойчивостью к сахарному диабету I типа, тогда как другие аминокислоты в этом положении (аланин, валин или серии) определяют восприимчивость.
Около 90% пациентов с сахарным диабетом I типа гомозиготны по аллелям DQB1, не кодирующим аспарагиновую кислоту в 57 положении. Раз молекула DQ, и конкретно 57 позиция р-цепи критична для связи антигена и пептида и Т-клеточного ответа, похоже, что различия в присоединении антигена, определяемые конкретной аминокислотой в 57 положении р-цепи DQ, непосредственно содействуют аутоиммунному ответу, уничтожающему инсулин-продуцирующие клетки поджелудочной железы. Тем не менее также важны другие локусы и аллели в МНС, что видно из того, что некоторые пациенты с сахарным диабетом I типа имеют в данной позиции b-цепи DQ аспарагиновую кислоту.
Гены, отличающиеся от локусов главного комплекса гистосовместимости класса II при сахарном диабете I типа
Гаплотип МНС отвечает только за часть генетического вклада в риск сахарного диабета I типа у сибсов пробанда. Семейные исследования показывают, что даже когда сибсы имеют те же гаплотипы МНС класса II, риск болезни составляет приблизительно 17%, что значительно ниже показателя конкордантности у однояйцовых близнецов, равного примерно 40%. Таким образом, в геноме должны быть другие гены, также предрасполагающие к развитию сахарного диабета I типа и различающиеся у однояйцовых близнецов и сибсов, имеющих аналогичные условия окружающей среды.
Кроме МНС, предполагают изменения еще в более чем десятке локусов, увеличивающих восприимчивость к сахарному диабету I типа, но надежно подтверждены только три из них. Это вариабельность числа тандемных повторов в промоторе гена инсулина и простой нуклеотидный полиморфизм в гене иммунного регулятора CTLA4 и в гене PTPN22, кодирующем протеин-фосфатазу. Идентификация других генов восприимчивости для сахарного диабета I типа как в пределах, так и за пределами МНС — объект интенсивного исследования. В настоящее время природа факторов негенетического риска при сахарном диабете I типа в основном неизвестна.
Генетические факторы сами по себе, тем не менее, не вызывают сахарный диабет I типа, поскольку показатель конкордантности у однояйцовых близнецов составляет не 100%, а только около 40%. До получения более полной картины участия генетических и негенетических факторов в развитии сахарного диабета I типа консультирование по оценке риска остается эмпирическим.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Неаутоиммунный сахарный диабет у детей
Сахарный диабет (СД) является серьезной проблемой современного здравоохранения во всем мире, влияющей на показатели здоровья, трудоспособности и, в конечном итоге, продолжительности жизни больших групп населения.
Сахарный диабет (СД) является серьезной проблемой современного здравоохранения во всем мире, влияющей на показатели здоровья, трудоспособности и, в конечном итоге, продолжительности жизни больших групп населения. Согласно определению, СД — это заболевание обмена веществ разной этиологии, которое характеризуется хронической гипергликемией, возникающей вследствие нарушения секреции, либо действия инсулина, либо обоих факторов одновременно [1, 2, 3]. Очевидно, что при сходстве финальных метаболических нарушений причины неэффективности действия гормона инсулина могут быть весьма многообразны. Поэтому для выбора адекватной терапевтической тактики важно не только диагностировать собственно диабет, но и максимально детализировать его этиологию.
В детской и подростковой популяции, длительное время считавшейся подверженной заболеваемости исключительно СД 1-го типа (СД 1), проблема дифференциальной диагностики представляется особенно актуальной. Статистика последних лет свидетельствует о возрастании вклада других типов СД в общую структуру заболеваемости СД у детей: СД 2-го типа (СД 2) — до 10%, моногенного СД (МГСД) — 1–3% [2, 3, 4, 5]. Эти данные нельзя считать окончательными в связи с ограничением доступности молекулярно-генетических методов обследования, а также сложившимися стереотипами в отношении диагностики СД у детей.
Между тем диагностические ошибки в установлении этиологии СД способны привести к неверной тактике в выборе терапии основного заболевания, планировании скрининга осложнений и коморбидных состояний и определении отдаленного прогноза. Известные в настоящее время варианты СД у детей, не относящиеся к 1-му типу, в большинстве своем не имеют четких патогномоничных проявлений, что затрудняет их диагностику, определяя необходимость анализа данных в совокупности, включая клинико-лабораторные симптомы, особенности дебюта и течения болезни, ответа на проводимую терапию [5, 6]. В связи с этим мы сочли целесообразным систематизировать современные сведения о неаутоиммунном СД у детей и предложить дифференциальный алгоритм, способный помочь практикующему врачу в диагностическом поиске.
Среди неаутоиммунных вариантов СД у детей можно выделить две основные группы — СД 2 и МГСД.
Сахарный диабет 2-го типа
СД 2 встречается примерно у 10% детей и подростков, больных диабетом. При диагностике следует учитывать особенности этого типа СД, которые должны рассматриваться в комплексе.
СД 2 у молодых имеет этнические особенности, превалируя у небелокожих европейцев, американцев и азиатов, но при этом может встречаться у лиц любой расы. По данным SEARCH for Diabetes in Youth (популяционное исследование среди 10–19-летних жителей США), СД 2 был диагностирован у 33% обследованных афроамериканцев, 22% латиноамериканцев, 40% жителей островов Тихого океана, 76% коренного населения США; при этом среди белых американцев встречался лишь у 6% обследованных. Статистика стран Восточной Азии свидетельствует о высокой заболеваемости СД 2 среди молодых: в Гонконге — до 90%, в Тайване — 50%, в Японии — 60%. Среди молодых жителей США и Европы СД 2 сильно коррелирует с избытком массы тела или ожирением, что не столь характерно для азиатов (в Японии, Индии, Тайване до 30% больных СД 2 детей и подростков имеют нормальный индекс массы тела) [4, 7, 8].
Манифест СД 2 у детей чаще приходится на второе десятилетие жизни (средний возраст — 13,5 лет), совпадая с пиком физиологической пубертатной инсулинорезистентности, которая, в свою очередь, может стать триггером манифестации ранее скрытого СД 2. Варианты клинического манифеста СД 2 широко варьируют. Возможно полное отсутствие клинических симптомов, и тогда СД 2 диагностируется при диспансерном обследовании пациентов из групп высокого риска или случайно. Однако примерно у трети больных в дебюте СД 2 имеет место кетоацидоз, что является частой причиной ошибочного установления диагноза СД 1. Описывается редкий вариант манифеста с развитием тяжелой дегидратации и гиперосмолярной комы с высоким риском летального исхода [9]. Гендерные различия ассоциированы с этническим фактором. Так, в популяции коренных американцев соотношение заболеваемости мальчиков и девочек соответствует 1:4–1:6, а в азиатской популяции подобные различия отсутствуют (1:1). Случаи заболеваемости СД 2 среди родственников, в том числе не первой степени родства, характерны для данного типа диабета. Однако у 15% детей с СД 2, в отличие от взрослых, может отсутствовать отягощенная наследственность [4, 8]. Данный факт наряду с возрастанием роли семейного анамнеза в диагностике СД 1 также может стать причиной ошибок в установлении типа СД у детей.
При СД 2, в отличие от СД 1, отсутствует ассоциация с HLA-маркерами и с аутоантителами.
СД 2, в основе патогенеза которого лежит инсулинорезистентность, может протекать изолированно, но чаще ассоциирован с другими составляющими метаболического синдрома: артериальной гипертензией, дислипидемией, центральным ожирением, acantosis nigricans, овариальной гиперандрогенией, неалкогольным жировым гепатозом (NAFLD), нефропатией. У девочек преждевременное (до 8 лет) изолированное адренархе повышает риск формирования впоследствии овариальной гиперандрогении. Артериальная гипертензия, по разным данным, встречается у 35–75% детей и подростков с СД 2. Нефропатия с симптомами микро- или макроальбуминурии может быть диагностирована как в дебюте, так и при длительном течении СД 2. Есть данные об исходе нефропатии при СД 2 в фокальный сегментарный гломерулосклероз. Дислипидемия характеризуется нарушением соотношения и ростом вклада атерогенных липидных фракций. При СД 2 у детей и подростков, ассоциированным с ожирением, могут иметь место признаки системного воспаления — повышение С-реактивного белка, уровня провоспалительных цитокинов, лейкоцитов, что в целом повышает суммарный кардиоваскулярный риск у взрослых [10, 11, 12, 13].
Установлено, что совокупность кардиоваскулярных факторов риска при наличии инсулинорезистентности и СД определяет высокий риск острых коронарных событий и повышает смертность среди взрослых лиц молодого возраста. Таким образом, СД 2 является серьезной патологией, имеющей особенности в популяции детей и подростков и требующей ранней диагностики, коррекции и своевременного скрининга специфических осложнений и коморбидных состояний [4, 14].
Подходы к ведению больных СД 2 во многом отличаются от таковых при более распространенном у детей СД 1. При сохранении основных компонентов терапии СД (диета, физические упражнения, медикаментозная терапия, обучение), в лечении СД 2 используется «ступенчатый» принцип. Выделяют три терапевтические ступени: диета и физические упражнения; диета, физические упражнения, метформин; диета, физические упражнения, метформин, инсулин.
Стартовая терапия СД 2 определяется клинической картиной и уровнем гликированного гемоглобина (HbA1c). При дебюте с отсутствием клинических симптомов и уровнем HbA1c 5 ммоль/л) приростом гликемии в ответ на углеводную нагрузку в стандартном оральном глюкозотолерантном тесте, сниженным почечным порогом, в связи с чем может определяться глюкозурия при нормогликемии, продолжительным (> 3 лет) периодом «медового месяца». Данные особенности затрудняют раннюю диагностику СД, что влияет на развитие сосудистых осложнений. Тактически пациенты с данным типом СД в дебюте могут получать только немедикаментозную терапию, но в дальнейшем нуждаются в присоединении фармакотерапии. Имеет место высокая чувствительность к препаратам сульфонилмочевины, которые в начале лечения назначаются в дозе, составляющей 1/4 от среднетерапевтической. У детей, нуждающихся в медикаментозной терапии, применяется инсулин [6, 25].
СД вследствие мутации гена HNF-4 альфа (MODY 1) по клиническим характеристикам подобен предыдущему варианту, но без нарушения почечного порога. Может быть диагностирован, когда имеют место клинические проявления MODY 3, но при генетическом исследовании не подтверждается мутация гена HNF-1 альфа [5, 6].
СД вследствие мутации гена глюкокиназы (MODY 2) сложен для диагностики из-за скудности проявлений. Наследуется по аутосомно-доминантному типу. Клинические симптомы, как правило, отсутствуют. Характерными являются длительная «мягкая» гликемия натощак (5–8,5 ммоль/л), высоконормальный или пограничный уровень HbA1c, невысокий прирост гликемии (
И. Л. Никитина, доктор медицинских наук
ФГУ «Федеральный центр сердца, крови и эндокринологии им. В. А. Алмазова» Росмедтехнологий, Санкт-Петербург
Генетические факторы развития сахарного диабета
Роль генетики в диагностике заболеваний
В настоящее время, благодаря развитию молекулярных методов исследования, разработано уже около 200 тестов, позволяющих выявлять наследственные предрасположенности к различным заболеваниям. Следует отметить, что исследования, направленные для выявления предрасположенности к развитию заболеваний, не ставят целью поставить диагноз, они лишь указывают на наличие генов, которые ассоциированы с заболеваниями.
 «Генетические маркёры» сахарного диабета
«Генетические маркёры» сахарного диабета
Показано, что ряд заболеваний может передаваться по наследству, а у части популяции имеются предпосылки для возникновения того или иного заболевания. Были обнаружены гены и их белковые продукты, которые отвечают за развитие таких заболеваний. В лабораторной практике иногда их называют «генетическими маркерами». Изучение таких маркёров дает возможность выделить группы различного риска развития заболеваний, и в частности, диабета. Такой подход может упростить раннюю диагностику заболевания (риск развития заболевания), до проявления основных клинических признаков.
При помощи генетических маркёров можно выявить группы людей с наличием риска развития сахарного диабета. Это является важным этапом диагностики диабета, поскольку в сочетании с традиционными методами (определение глюкозы, гликированного гемоглобина, и т.д.) приводит к улучшению диагностики заболевания еще до проявления выраженных клинических симптомов заболевания и помогает разработке поведения человека и принятия профилактических мер.
Помимо моногенных наследственных заболеваний, обусловленных мутациями в определенном гене, ответственным за кодирование какого-либо белка, часть заболеваний является мультифакторными или сложно наследуемыми. Это означает, что заболевание может реализоваться в результате деятельности нескольких генов, а также в результате воздействия других причин, например, воздействия окружающей среды. К мультифакторным заболеваниям относят: сахарный диабет, остеопороз, атеросклероз, ишемическую болезнь сердца, злокачественные новообразования. К генетически детерминируемым состояниям можно отнести ожирение, склонность к алкоголизму.
Генетика сахарного диабета 2 типа
Генетика сахарного диабета 1 типа
В статье представлен анализ литературных данных по современным исследованиям в области генетической предрасположенности к сахарному диабету. Проведена попытка обобщить полученные за последние несколько лет данные в единую гипотезу, учитывающую генетические, иммунологические и внешние факторы, влияющие на развитие сахарного диабета 1 типа.
Genetics of Type I Diabetes
Ryzhkov P. A., Ryzhkova N. S., Konovalova R. V.
Analysis of literary data on modern researches in the field of genetic predisposition to diabetes in article is presented. The data that obtained for the last years attempt was generalized and spent to the uniform hypothesis considering genetic, immunologic and external factors that influence to development of a type 1 diabetes.
Введение
На сегодняшний день сахарный диабет занимает первое место по распространенности среди эндокринных заболеваний. В мире насчитывается около 135 млн. больных сахарным диабетом и их количество ежегодно увеличивается на 5—7% [2]. В общем по состоянию на 2010 год число больных сахарным диабетом на нашей планете составляло 285 млн. человек, а к 2030 году предположительно удвоится [33]. В разных странах и регионах распространенность СД значительно варьирует. Известно, что заболеваемость СД 1 типа увеличивается с юга на север и с востока на запад. Высокий уровень заболеваемости отмечается в Скандинавских странах (Финляндии, Швеции, Дании), а наиболее редко СД встречается в странах Востока (Корея, Япония). В России число больных сахарным диабетом на 2010 г. составляло чуть более 3 млн человек и, согласно прогнозу, за ближайшие два десятилетия будет зарегистрировано 5,81 млн больных, при этом такое же число больных не будет выявлено [6]. Сахарный диабет относится к мультифакториальным заболеваниям, его развитие обусловлено сочетанием генетической предрасположенности и действием неблагоприятных факторов внешней среды. Т. к. за последнее время накопилось большое количество данных о влиянии генетических факторов на развитие сахарного диабета, является целесообразным их обобщить и представить цельную картину, сложившуюся на сегодняшний день в области изучения генетики сахарного диабета. Различают генетически (наследственно) обусловленные и не обусловленные генетически формы сахарного диабета. Генетически обусловленный сахарный диабет неоднороден. С учетом патогенеза можно выделить условно инсулинозависимый (I тип) и инсулиннезависимый (II тип) диабета. Данная статья посвящена первому типу сахарного диабета.
I тип сахарного диабета
Сахарный диабет I типа является аутоиммунным заболеванием, для которого характерны следующие клинические признаки: высокая степень гипергликемии, присутствие гипокликемий и кетоацидоза при декомпенсации диабета, стремительное развитие инсулиновой недостаточности (в течение 1—2-х недель) после манифестации заболевания. Инсулиновая недостаточность при СД 1 типа обусловлена практически полной деструкцией β-клеток поджелудочной железы, ответственных за синтез инсулина в организме человека. Несмотря на большое количество исследований в этой области, до сих пор остаётся непонятным механизм развития сахарного диабета 1 типа. Считается, что инициирующим фактором развития СД1 типа является повреждение β-клеток поджелудочной железы действием одного или нескольких неблагоприятных факторов окружающей среды (рис. 1). К таким факторам относятся некоторые вирусы, токсические вещества, копчёные продукты, стрессы. Данную гипотезу подтверждает наличие аутоантител к антигенам островка поджелудочной железы, которые, по мнению большинства исследователей, являются свидетельством аутоиммунных процессов в организме и непосредственно не вовлечены в механизмы деструкции β-клеток. Кроме того, наблюдается закономерное снижение количества аутоантител по мере удлинения срока от начала развития диабета I типа. Если в первые месяцы от начала заболевания антитела выявляются у 70—90 % обследованных, то через 1—2 года от начала болезни — лишь у 20 %, при этом аутоантитела выявляются также до клинической манифестации диабета 1 типа и у родственников больных, причем наиболее часто у родственников, имеющих идентичные системы HLA [22]. Аутоантитела к антигенам островков поджелудочной железы являются иммуноглобулинами класса G. Следует указать, что при диабете I типа антитела класса IgM или IgA не обнаруживаются даже в случаях остро развившегося заболевания. В результате деструкции β-клеток высвобождаются антигены, которые запускают аутоиммунный процесс. На роль таковых, активирующих аутореактивные Т-лимфоциты, претендуют несколько различных аутоантигенов: препроинсулин (PPI), глутаматдекарбоксилаза (GAD), инсулинома-ассоциированный антиген 2 (I-A2) и цинковый транспортер (ZnT8) [30, 32].

Рисунок 1 — Предположительная схема развития СД 1 типа с учетом генетических и внешних факторов
После повреждения β-клеток на их поверхности начинают экспрессироваться молекулы HLA 2 класса, обычно не представленные на поверхности неиммунных клеток. Экспрессия HLA-антигенов класса 2 неиммунными клетками превращает последние в антигенпрезентирующие и подвергает серьезной угрозе их существование. Причина аберрантной экспрессии МНС-белков класса 2 соматическими клетками до конца не ясна. Однако показано, что при длительной экспозиции in vitro β-клеток с γ-интерфероном такая экспрессия возможна. Применение йода в местах его эндемии сопровождается аналогичной экспрессией МНС-белков класса 2 на тиреоцитах, что приводит к увеличению числа больных аутоиммунным тиреоидитом в этих областях. Данный факт доказывает также роль факторов внешней среды в возникновении аберрантной экспрессии МНС-белков класса 2 на β-клетках. Принимая во внимание вышеназванные факты, можно предположить, что особенности аллельного полиморфизма HLA-генов у конкретных индивидуумов влияют на способность β-клеток экспрессировать МНС-белки 2 класса и, таким образом, на предрасположенность к сахарному диабету 1 типа.
Кроме того, относительно недавно было установлено, что инсулинпродуцирующие β-клетки экспрессируют на своей поверхности MHC-белки класса 1, которые презентируют пептиды цитотоксическим CD8+ Т-лимфоцитам [34].
Роль Т-лимфоцитов в патогенезе СД1
С другой стороны, полиморфизм генов системы HLA определяет селекцию Т-лимфоцитов при созревании в тимусе. При наличии определенных аллелей генов системы HLA, по-видимому, не происходит элиминации Т-лимфоцитов, которые несут на своей поверхности рецепторы к аутоантигену (-ам) β-клеток поджелудочной железы, тогда как в здоровом организме такие Т-лимфоциты уничтожаются на стадии созревания. Таким образом, при наличии предрасположенности к СД 1 типа в крови циркулирует некоторое количество аутореактивных Т-лимфоцитов, которые активируются при определённом уровне аутоантигена (-ов) в крови. При этом уровень аутоантигена (-ов) повышается до порогового значения либо в результате прямого разрушения β-клеток (хим. веществами, вирусами) либо наличием в крови вирусных агентов, чьи антигены имеют перекрестную реакцию с антигенами β-клеток поджелудочной железы.
Необходимо отметить, что в регуляции активности аутореактивных Т-лимфоцитов непосредственное участие принимают Т-регуляторные клетки (Treg), обеспечивающие таким образом поддержание гомеостаза и аутотолерантности [16, 29]. Т. е. Treg клетки выполняют функцию защиты организма от аутоиммунных заболеваний [7]. Регуляторные Т-клетки (Tregs) активно участвуют в поддержании аутотолерантности, иммунного гомеостаза и противоопухолевого иммунитета. Считается, что они играют существенную роль в прогрессировании рака. Их число коррелирует с более агрессивным статусом заболевания и позволяет прогнозировать время лечения. Кроме того, нарушение регуляции функции или частоты Tregs клеток может привести к множеству аутоиммунных заболеваний, включая сахарный диабет 1 типа.
Treg клетки представляют собой субпопуляцию Т-лимфоцитов, экспрессирующих на свой поверхности рецепторы к интерлейкину 2 (т. е. они являются CD25+) [28]. Однако, CD25 не являются исключительно специфическими маркером Treg клеток, поскольку его экспрессия на поверхности эффекторных Т-лимфоцитов происходит после активации [25]. Основным маркером Т-регуляторных лимфоцитов является экспрессирующийся на поверхности клеток внутриклеточный транскрипционный фактор FoxP3, также известный как IPEX или XPID [9, 14, 26]. Он является важнейшим регуляторным фактором, отвечающим за развитие и функционирование Т-регуляторных клеток. Кроме того, экзогенный IL-2 и его рецептор играют ключевую роль в выживании Treg клеток на периферии [27].
Также есть предположение, что аутоиммунный процесс запускается не самим разрушением β-клеток, а их регенерацией вследствие такого разрушения [1].
Генетическая предрасположенность к сахарному диабету
Таким образом, основной генетический вклад в предрасположенность к сахарному диабету 1 типа вносят гены системы HLA, а именно гены, кодирующие молекулы 2 класса главного комплекса гистосовместимости человека. В настоящее время существует не более 50 HLA регионов, которые существенно влияют на риск развития сахарного диабета типа 1. Многие из этих регионов содержат интересные, но ранее неизвестные гены кандидаты. Генетические области, обладающие связью с развитием сахарного диабета 1 типа, принято обозначать локусами ассоциации IDDM. Кроме генов системы HLA (локус IDDM1), значительной ассоциацией с СД 1 типа обладает генная область инсулина на 11p15 (локус IDDM2), 11q (локус IDDM4), 6q и, возможно, область на хромосоме 18. Возможные гены кандидаты в пределах областей связи включают (GAD1 и GAD2, которые кодируют фермент глутаматдекарбоксилазу; SOD2, который кодирует супероксиддисмутазу; и локус группы крови Kidd), вероятно, играют важную роль [8].
Другие важные локусы, ассоциированные с СД1 представляют собой ген PTPN22 на 1p13, CTLA4 на 2q31, рецептор интерлейкина-2 α (CD25, кодируемых IL2RA) локус 10p15, IFIH1 (также известный как MDA5) на 2q24 и совсем недавно открытые CLEC16A (KIAA0350) на 16p13, PTPN2 на 18p11 и CYP27B1 на 12q13 [31].
Ген PTPN22 кодирует белок лимфоидную тирозинфосфатазу также называемую LYP. PTPN22 непосредственно связан с активацией Т-клеток. LYP подавляет сигнал Т-клеточного рецептора (TCR) [13]. Данный ген можно использовать в качестве мишени для регуляции функции Т-клеток, поскольку он выполняет функцию торможения TCR сигнализации.
Ген CTLA4 кодирует ко-рецепторы на поверхности клеток Т-лимфоцитов. Он также является хорошим кандидатом для воздействия на развитие СД1, поскольку негативно влияет на активацию Т-клеток [21].
Ген рецептора интерлейкина 2α (IL2RA) состоит из восьми экзонов и кодирует α цепь IL-2 рецепторного комплекса (также известного как CD25). IL2RA играет важную роль в регуляции иммунитета. IL2RA экспрессируется на регуляторных Т-клетках, что, как уже говорилось выше, имеет важное значение для их функционирования, и соответственно для подавления Т-клеточного иммунного ответа и аутоиммунных заболеваний. Эта функция гена IL2RA, свидетельствует о его потенциальной роли в патогенезе СД1, вероятно, с участием регуляторных Т-клеток [20].
Ген CYP27B1 кодирует витамин D 1α-гидроксилазы. Из-за важной функции витамина D в регуляции иммунитета, он рассматривается как ген-кандидат. Элина Хиппонен с сотрудниками установили, что ген CYP27B1 связан с СД1. Ген, вероятно, включает в себя механизм воздействия на транскрипцию. В результате исследований было показано, что витамин D может каким-то образом подавлять аутоиммунные реакции, ориентированные на β-клетки поджелудочной железы. Эпидемиологические данные показывают, что добавки витамина D могут помешать развитию СД1 [15].
Ген CLEC16A (ранее KIAA0350), который экпрессируется почти исключительно в иммунных клетках и кодирует последовательность белка области лектина типа C. Экспессируется в-лимфоцитах, как специализированные APCs (антиген-презентирующие клетки). Особенно интересно, что лектины типа C, как известно, играют важную функциональную роль в поглощении антигена и презентации β клеток [11].
Генетический анализ модели инсулинозависимого диабета ассоциированного с главным комплексом гистосовместимости у мышей показал, что в развитии заболевания основную роль играет главный комплекс гистосовместимости во взаимодействии с 10 другими локусами предрасположенности в различных местах генома [23].
Полагают, что система HLA является генетической детерминантой, которая определяет предрасположенность β-клеток поджелудочной железы к вирусным антигенам, или отражает степень выраженности противовирусного иммунитета. Установлено, что при инсулинозависимом сахарном диабете часто обнаруживаются антигены В8, Bwl5, B18, Dw3, Dw4, DRw3, DRw4. Показано, что наличие у пациентов HLA-антигенов В8 или В15 повышает риск заболеваемости сахарным диабетом в 2–3 раза, а при одновременном присутствии В8 и В15 — в 10 раз. При определении гаплотипов Dw3/DRw3 риск заболеваемости сахарным диабетом увеличивается в 3,7 раза, Dw4/DRw4 — в 4,9, a Dw3/ DRw4 — в 9,4 раза [1].
Основными генами системы HLA, ассоциированными с предрасположенностью с развитием СД1 типа являются гены HLA-DQA1,HLA-DQA, HLA-DQB1, HLA-DQB, HLA-DRB1, HLA-DRA и HLA-DRB5. Благодаря обширным исследованиям в России и по всему миру, было установлено, что различные сочетания аллелей генов системы HLA по разному влияют на риск развития сахарного диабета 1 типа. Высокая степень риска связана с гаплотипами DR3 (DRB1 *0301-DQA1*0501-DQB*0201) и DR4 (DRB1*0401,02,05-DQA1*0301-DQB1*0302). Средняя степень риска сочетается с гаплотипами DR1 (DRB1*01-DQA1*0101-DQB1 *0501), DR8 (DR1*0801-DQA1*0401-DQB1*0402), DR9 (DRB1*0902-DQA1*0301-DQB1*0303) и DR10 (DRB2*0101-DQA1*0301-DQB1*0501). Кроме того, установлено, что некоторые аллельные сочетания имеют защитное действие по отношению к развитию диабета. К таким гаплотипам относятся DR2 (DRB1*1501-DQA1*0102-DQB1*0602), DR5 (DRB1*1101-DQA1*0102-DQB1 *0301) — высокая степень защиты, DR4 (DRB1*0401-DQA1*0301-DQB1*0301); DR4 (DRB1*0403-DQA1 *0301-DQB1*0302) и DR7 (DRB1*0701-DQA1*0201-DQB1*0201) — средняя степень защиты [3]. Следует отметить, что предрасположенность к развитию СД 1 типа зависит от популяции. Так, некоторые гаплотипы в одной популяции обладают выраженным протективным действием (Япония), а в другой ассоциируются с риском (Скандинавские страны).
В результате проводимых исследований всё время открываются новые гены, обладающие связью с развитием СД 1 типа. Так, при анализе в шведских семьях по 2360 SNP маркёрам в пределах локуса главного комплекса гистосовместимости и смежных с ним локусах в области центромеры были подтверждены данные об ассоциации СД 1 типа с локусом IDDM1 в главном комплексе гистосовместимости человека, наиболее выраженной в области HLA-DQ/DR. Также, было показано, что в центромерической части пик ассоциации приходился на генетическую область, кодирующую инозитол 1, 4, 5-трифосфат рецептор 3 (ITPR3). Предполагаемый популяционный риск для ITPR3 составил 21,6 %, что свидетельствует о важном вкладе гена ITPR3 в развитие сахарного диабета 1 типа. Двухлокусовый регрессионный анализ подтвердил влияние изменения гена ITPR3 на развитие СД 1 типа, при этом данный ген является отличным от любого гена, кодирующего молекулы второго класса главного комплекса гистосовместимости [24].
Как уже говорилось, кроме генетической предрасположенности на развитие сахарного диабета 1 типа влияют внешние факторы. Как показали последние исследования на мышах, одним из таких факторов является передача иммуноглобулинов от больной аутоиммунной матери потомству. В результате такой передачи у 65% потомства развивался диабет, в то же время при блокировании передачи иммуноглобулинов матери потомству, в потомстве заболевало только 20 % [17].
Генетическая взаимосвязь СД 1 и 2 типов
Недавно были получены интересные данные о генетической связи между первым и вторым типами сахарного диабета. Li с соавторами (2001) оценили распространенность семейств с обоими типами диабета в Финляндии и изучили, у больных с типом II диабет, ассоциации между семейной историей 1 типа диабета, антителами к глютаматдекарбоксилазе(GADab), и ассоциированные с первым типом диабета генотипы HLA-DQB1. Затем, в смешанных семействах с 1 и 2 типом диабета, они изучали, влиял ли общий гаплотип HLA у членов семьи с диабетом 1 типа на проявление диабета 2 типа. Среди 695 семей, в которых было более 1 пациента со 2 типом диабета, 100 (14 %) также имели родственников с диабетом 1 типа. Пациенты со вторым типом диабета из смешанных семейств, чаще имели GAD-антитела (18 % против 8 %) и генотип DQB1*0302/X (25% против 12 %), чем пациенты из семейств с диабетом только 2 типа; однако, у них была более низкая частота генотипа DQB1*02/0302 по сравнению со взрослыми пациентами с 1 типом диабета (4 % против 27 %). В смешанных семействах инсулиновый ответ на нагрузку глюкозой был хуже у больных, имеющих рисковые гаплотипы HLA-DR3-DQA1*0501-DQB1*02 или DR4*0401/4-DQA1*0301-DQB1*0302, по сравнению с пациентами без таких гаплотипов. Это обстоятельство не зависело от наличия GAD-антител. Авторы заключили, что 1 и 2 типы диабета кластеризуются в одних и тех же семействах. Общий генетический фон у пациентов с диабетом 1 типа предрасполагает диабетиков 2 типа и к наличию аутоантител и, независимо от наличия антител, к сниженной секреции инсулина. Их исследования также подтверждают возможное генетическое взаимодействие между 1 типом диабета и 2 типом диабета, обусловленное локусом HLA.
Заключение
В заключение можно отметить, что за последние 10 лет исследователи сильно продвинулись в изучении генетики и механизма развития сахарного диабета 1 типа, однако до конца остается невыясненным механизм наследования предрасположенности к СД 1 типа, также нет стройной теории развития сахарного диабета, которая бы объясняла все полученные в этой области данные. Представляется, что основным направлением в изучении сахарного диабета в настоящее время должно стать компьютерное моделирование предрасположенности к СД, учитывающее различную диабетогенность аллелей в различных популяциях и их связь между собой. При этом наиболее интересными с точки зрения возникновения СД 1 типа может являться изучение механизмов: 1) избегания гибели аутореактивных Т-лимфоцитов в процессе селекции в тимусе; 2) анормальной экспрессии β-клетками молекул главного комплекса гистосовместимости; 3) нарушения баланса между аутореактивными и регуляторными Т-лимфоцитами, а также поиск функциональных связей между локусами ассоциации с СД 1 типа и механизмами развития аутоиммунитета. Учитывая результаты последних исследований, можно с известной долей оптимизма предположить, что полное раскрытие генетических механизмов развития сахарного диабета и его наследования уже не очень далеко.
